地球表面的70.8%为海洋所覆盖。海洋的面积为361×10°平方公里,其平均深度为3800米。因此海水所占的体积为1372×10°立方公里,若海水的平均密度以1.03计,则海水的重量为1.413×1021克。据据戈德施密特(V.M.Go-Idshmidt,1954)推算,地球上每一平方厘米存有273升水,其细节如表1.1所示,海水占地球表面全部水体的98%以上。

此外,如表1.2所示,因为水圈中的水量为存在于地球总水量的62.5%,所以这就是说,海水的量占地球存在总水量的近2/3。
表1.1地球表面上存在的各种水的数量
升/厘米2 %
海水 268,45 98.8
淡水 0,1 0.037
大陆冰 4.5 1,65
水蒸气 0.003 0,001
由海洋、河流、湖沼、陆地等表面蒸发的水蒸气,变成雨或雪后又返回到地面。降到陆地上的雨以河水的形式注入海洋,或滲透到地球内部。降到极地区域的雪变成了万年积雪,并终究变成冰河注入海洋。估计计全球水的年蒸发量为0.083升/厘米2(A. Defant1961),因此,就可算出水蒸气每10天,淡水每1年更换一次。这样,激烈地循环在地表的水使地球上一切物质受到变化。河水在地表溶解岩石,边溶存盐类,边把沙土搬运到海中。另外,渗渗进地壳的水在高温高压下与岩石反应,复以温泉水形式涌出。
表1.2地球上存在的水量(1021克)
水圈 1413
岩石圈圖(堆积岩) 90
花岗岩) 20
(玄武岩) 730
地球上的生物,不论是动物还是植物,都需要水,水为其体内主要组成要素。例如,人体内约70%,陆栖动物体内50~75%,水栖植物体内95%以上是水。由此可想而知水对于生物是不可缺少的,并且维持生命的反应,总是在体内的水溶液中,以酶为催化剂缓慢地进行着。比如,植物以太阳光为能量,在叶绿素的作用下,由水和二氧化碳合成碳水
表1.3水的异常性质及其在自然界的意义
性质 与其它化合物比较 在自然界中的意义
沸点,融融点 在第六族元素的氢化物中特别高 常温下以液体存在
融解热 最高(除NHs外) 起0℃恒温槽作用
蒸发热 最高 起恒温槽作用
密度 4℃时最高 对海水、湖水温度垂直分布是重要的
表面张力 最高 对细胞生理是重要的
介电常数 最高 在以水为溶剂的性质方面起作用
电离度 小 对H+,OH有影响
导热性 最高 在细胞中是重要的
化合物而使其生长。对水栖动物来说,水本身身是其生活的场所,就是对陆梄动物来讲,水的存在也决定其栖息的条件。对人类来说,水也是生活所必需的,作为工业用水也具有重要的意义。
这样一来,水是地球上最常见的物质之一,对生命更是不可缺少的。水为什么在地球上占有如此特殊的地位呢?就周期表来看,元素按原子量的顺序排列,按一定规律,其化合物的性质相似,并且依次变化着。这个事实可用于推测未发现元素的化合物性质,在发现元素方面是有用的。就水本身来说也有与之极相类似的化合物,也应当有能代替它的物质。可是,如如从物理化学方面越详加比较,水的性质越是显得与其它化合物不同。在表1.3中,示出了它们的性质及其在自然界中的意义。而且,似乎可以说正是水的这些与众不同的性质决定了它在地球上的重要性。本编,在论述海水之前,试想在第一章和第二章从物理化学方面对组成水、海水的水分子作一研究,这大概在理解纯水、海水的性质方面是最有效的方法。
水分子组成
众所周知,水分子由一个氧原子和两个氢原子构成。氢有三种天然存在的同位素(1H,2H(D),3H(T),氧有六种同位素(14O,15O,16O,17O,18O,19O)。它们的存在比和半衰期示于表1.4。其中,H主要由宇宙射线和氮原子在
高空碰撞生成的,但在地球上的浓度则随条件而迴然不同此外,由于14O,150和19O的半衰期都很短,所以它们在地球上几乎不存在。天然存在的水是含有这些同位素的混合物,其各种分子的浓度示于表1.4中,其中大部分都是1H2 16O这一种。书中论述水的性质时,就意味着论述这些同位素混合物的性质。
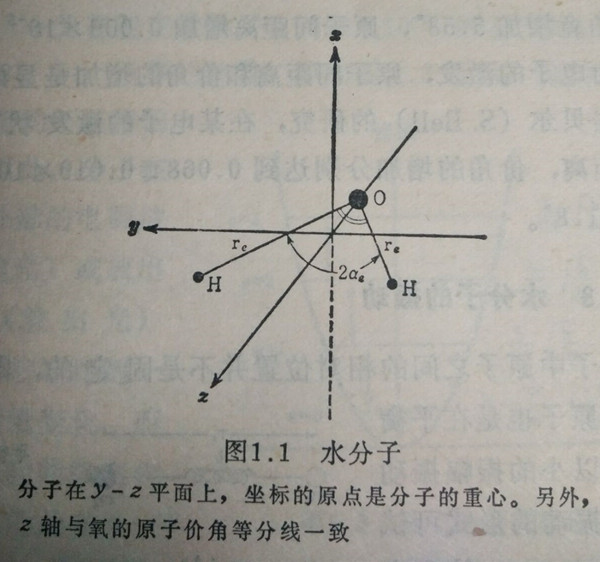
水分子的构造
如图1.1所所示,水分子结构的形状是以氧原子为顶点的等腰三角形,许多研究者对O一H原子间的距离以及氧原子的价角进行了正确的测定。三种主要水分子的原子间距离,
表1.4氢氧的同位素与水的主要分子形式
元素 同位素 存在比 半衷期
氢 轻氢( Protium)1H(H) 99.98%
重氢( Deuterium)2HD 0.0157%
超重氢( Tritium)H(T) ~10-18CT/H) 12.5年
氧 14 O
15 O
16 O 99.759%
17 O 0.0374
18 O 0.1994%
19 O
分子种类 存在比(%)
H2160 99.73
H2180 0,20
H2170 0.037
HD180 0,03