



































![双[3-(三乙氧基甲硅烷基)丙基]四硫化物](images/202306/thumb_img/5073_thumb_G_1686793139947.jpg)






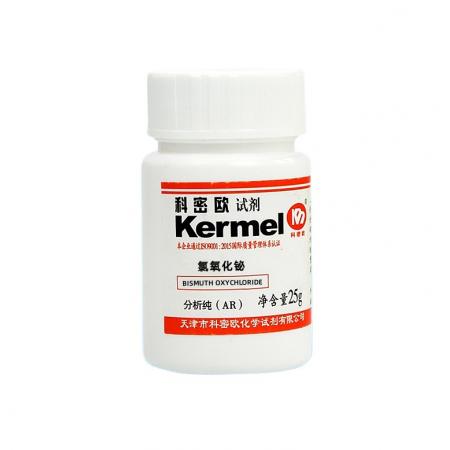
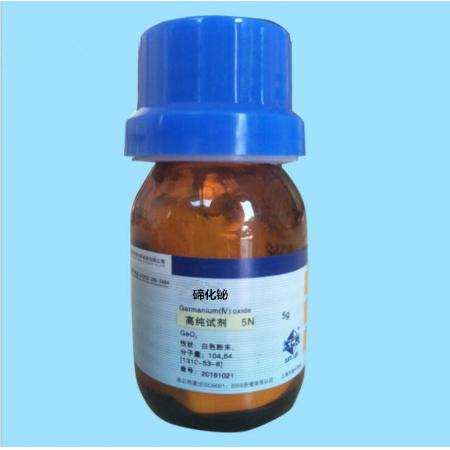
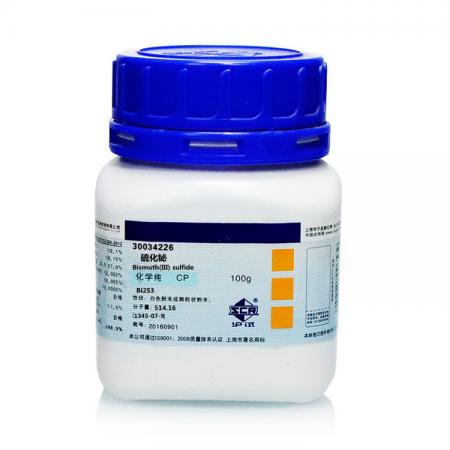
在砷、锑、铋的M3+盐溶液中或用强酸酸化后的MO33-、MO43-溶液中通入H2S都可得到有颜色的相应的硫化物沉淀,见表13-8砷分族元素硫化物的颜色和它们在酸碱溶液中的溶解性。
表13-8 砷、锑、铋硫化物的颜色和溶解性
| 硫化物 | As2S3 | As2S5 | Sb2S3 | Sb2S5 | Bi2S3 |
| 颜色 | 黄色 | 黄色 | 橙红 | 橙红 | 棕黑 |
| 在浓HCl中 | 不溶 | 不溶 | 溶 |
溶* Sb(Ⅴ) →Sb(Ⅲ) |
溶 |
| 在NaOH中 | 溶 | 溶 | 溶 |
溶 |
不溶 |
| 在Na2S或(NH4)2S中 | 溶 | 易溶 | 溶 | 易溶 | 不溶 |
* Sb2S5+6H++8Cl-=2SbCl4-+3H2S↑+2S↓
砷分族硫化物的酸碱性与相应的氧化物很相似。As2S3和Sb2S3显两性,前者两性偏酸性不溶于浓HCl、只溶于碱,而后者既溶于酸又溶于碱。Bi2S3显碱性不溶于碱。
AS2S3+6OH-=AsO33-+AsS33-+3H2O
Sb2S3+6OH-=SbO33-+SbS33-+3H2O
Sb2S3+6H++12Cl-=2[SbCl6]3-+3H2S↑
AS2S3和Sb2S3还能溶于碱性硫化物如Na2S或(NH4)2S中,而Bi2S3不溶。
As2S3+3S2-=2AsS33-
.jpg)
硫代亚砷酸盐可看做是亚砷酸盐中的O被S所取代的产物,上面这个反应就好象具有酸性的氧化物能溶解在碱中一样:
As2O3+6OH-=2AsO33-+3H2O

As2S5和Sb2S5的酸性分别比相应的M2S3强,因此,M2S5比M2S3更易溶于碱性硫化物溶液中。
As2S3和Sb2S3都具有还原性,与多硫化物反应生成硫代酸盐,而Bi2S3的还原性极弱不与多硫化物作用。
As2S3+3S22-=2AsS43-+S
砷、锑的硫代酸盐和硫代亚酸盐与酸反应时生成硫代酸和硫代亚酸,它们很不稳定,在生成时就分解放出H2S并析出硫化物。
2AsS43-+6H+=As2S5↓+3H2S↑
2AsS33-+6H+=As2S3↓+3H2S↑
