






















砷、锑、铋的氧化物有两类:氧化数为+Ⅲ的有As2O3、Sb2O3和Bi2O3,氧化数为+Ⅴ的有As2O5和Sb2O5。直接燃烧砷锑铋单质能得到M2O3,而M2O5则是由其单质用浓硝酸氧化所得的相应水合物脱水而制得。
4M+3O2=M4O6(M为As、Sb)
4Bi+3O2=2Bi2O3
3As+5HNO3+2H2O=3H3AsO4+5NO
6Sb+10HNO3+3xH2O=3Sb2O5·xH2O+10NO↑+5H2O
Sb2O5·xH2O=(加热)Sb2O5+xH2O
硝酸只能把铋氧化成Bi(NO3)3,
Bi+4HNO3=Bi(NO3)3+NO+2H2O
五氧化二铋只有在碱性介质中用较强的氧化剂如Cl2氧化Bi(Ⅲ)化合物生成NaBiO3
Bi(OH)3+Cl2+3NaOH=NaBiO3+2NaCl+3H2O
以酸处理NaBiO3则得红棕色的Bi2O5,它极不稳定很快地分解为Bi2O3和O2。
As2O3是砷的重要化合物,俗称砒霜,是剧毒的白色粉状固体,致死量为0.1g。As2O3中毒时,可服用新制的Fe(OH)2(用MgO和FeSO4溶液强烈摇动制得)悬浮液来解毒。可用于制造杀虫剂、除草剂以及含砷药物。As2O3微溶于水生成亚砷酸,亚砷酸仅存在于溶液中。As2O3是两性偏酸性氧化物,因此它易溶于碱,生成亚砷酸盐。

砷(Ⅲ)、锑(Ⅲ)、铋(Ⅲ)的氧化物水合物的酸碱性与它们的氧化物相似,按照H3AsO3—Sb(OH)3—Bi(OH)3顺序酸性依次减弱。现将砷分族元素氧化物及其水合物的酸碱性归纳于表13-7。
表13-7 砷、锑、铋氧化物及其水合物的酸碱性
| 砷 | 锑 | 铋 | ||
| 氧化数 | +Ⅲ |
As2O3 H3AsO3 两性偏酸性 |
Sb2O3 Sb(OH)3 两性 |
Bi2O3 Bi(OH)3 弱碱性 |
| 氧化数 | +Ⅴ |
As2O5 H3AsO4 弱酸性 |
Sb2O5 H[Sb(OH)6] 两性偏酸性 |
— |
| 酸碱性的递变规律 |
(1)从As到Bi碱性递增酸性递减; (2)同一元素+Ⅴ氧化态的酸性比+Ⅲ氧化态的强。 |
As(Ⅲ)、Sb(Ⅲ)、Bi(Ⅲ)的卤化物和其它强酸所形成的盐,在溶液中都强烈地水解,因为它们相应的氧化物的水合物不是弱酸便是弱碱。例如卤化砷水解后生成相应的氢卤酸和亚砷酸。
AsX3+3H2O=H3AsO3+3HX
锑和铋的氧化数为+Ⅲ的盐水解后生成难溶的锑和铋的酰基盐:
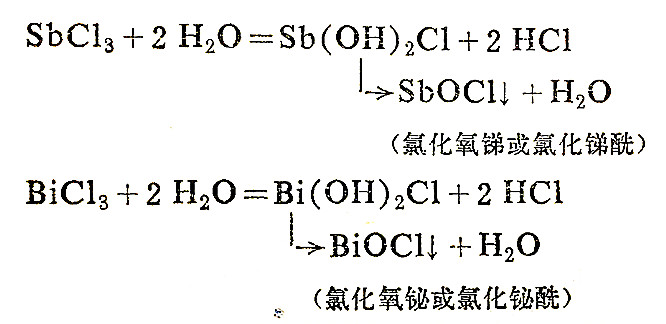
随着As—Sb—Bi顺序碱性逐渐增强,共水解程度逐渐减弱。由于Sb(Ⅲ)和Bi(Ⅲ)的酰基盐是难溶的,所以锑和氧化数为+Ⅲ的盐在常温时水解进行得并不完全,通常就停留在酰基盐的阶段。
砷分族按As—Sb—Bi顺序+Ⅲ氧化态的特征逐渐增强,形成稳定的Bi(Ⅲ)化合物是铋的特征。氧化态为+Ⅴ的铋酸钠是一种很强的氧化剂,能把Mn2+离子氧化为MnO4-离子。
2Mn2++5BiO3-+14H+=2MnO4-+5Bi3++7H2O
而砷的氧化数为+Ⅲ的亚砷酸盐是还原剂,能还原象碘这样弱的氧化剂,
AsO33-+I2+2OH- ⇋AsO43-+2I-+H2O
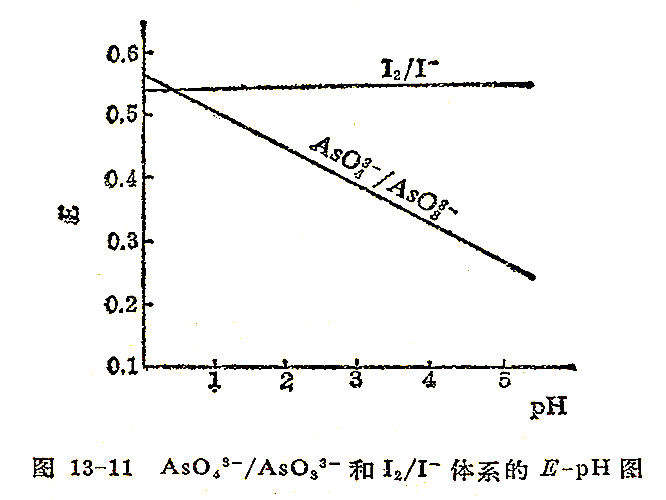
上述这两个反应都与溶液的酸度有关,后一反应必须在弱酸性介质中才能进行,若溶液的酸性较强,反应的方向会发生改变,I2就不可能氧化AsO33-,因为电对AsO43-/AsO33-的电极电势数值随着溶液pH值的降低而变大。
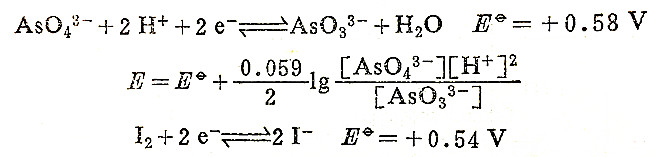
电对I2/I-的电极电势在一定pH范围内无变化。这两个电对的电极电势随溶液的pH而变化的情况见图13-11。从图中可看出,在较强酸性溶液中H3AsO4可以氧化I-,而在弱酸性时H3AsO3才可能还原I2,实际上,反应是在pH=5~9时较为适宜,pH小于4反应不完全,pH大于9时会引起I2的歧化反应。
总之,砷、锑、铋三元素的氧化态为+Ⅲ的化合物具有还原性,氧化态为+Ⅴ的化合物具有氧化性,其变化规律如下:
