




















如果我们假定在同温和同压条件下,对所有的气体来说,等体积中含有相同数目的分子。气体的化合体积定律可以满意地用气体的分子理论来加以解释,亚佛加德罗在1811年发展了这个假说来说明气体的性质。他的假说后来被实验所证实,现已成为为事实即熟知的亚佛加德罗定律。
考虑氢气和氯气化合生成氯化氢气的反应,反应物和生成物的体积是在同温和同压条件下测定的:
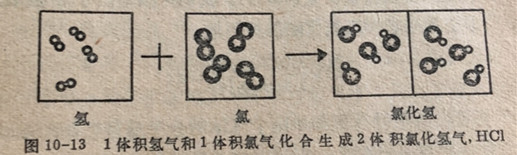
1体积的H2+1体积的Cl2→2体积的HC1
根据亚佛加德罗定律,同体积的氢气、氯气和氯化氢气含有相同数目的分子。于是在反应过程中一个氢分子和一个氯分子反应生成两个氯化氯分子。现在每个氯化氢分子必须至少包含一个氢原子和一个氯原子;因此,两个氯化氢的分子至少要包含两个氢原子和两个氯原子,那么在每一个氢分子和每一个氯分子中必定都各含有两个原子
1体积的H2+1体积的C12→2体积的HC1
1分子的H2+1分子的C12→2分子的HC1
现在还没有发现过这样的一种气体反应,即在其中一个氢(或氯)分子含有多个元素原子而能生成多于两个分子的产物。因此,我们假定,每个氢(或氯)分子包含两个并且仅能包含两个原子。如果可能把1份氢气样品中所有的双原子分子都分解解成单原子分子,我们将可预期在同温和同压条件下体积将加倍。每个原来的氢分子将分解成两个新的分子。
H2(1体积)→2H(2体积)
可以类似地证明氧、氮、氟、氯、溴和碘等也是由双原子分子构成的。
由氢和氯生成氯化氢所涉及的体积关关系可以表示如图10-13。其它气体反应都能遵守盖吕萨克定律可以类似于氢和氯的反应用作图的方法来加以说明。在盖吕萨克定律以前道尔顿考虑到了但随后又否定了同体积的气体含有相相同数目原子的思想;他那时没有想到单质可以存在为多原子分子(例如H2,O)。
盖吕萨克定律可以用来求在反应中气体的体积。
