























两个锂原子结合起来形成一个锂分子Li2是和H2的形成相类似的,不同的是在原则上仅涉及2s原子轨道而不是18轨道。每
个锂原子的电子结构是1s22s1,有一个价电子。因此,有两个价电子可以占入o2s。成键分子轨道中。各原子在较低能量状态18轨道中的18电子在成键过程中不起什么作用。
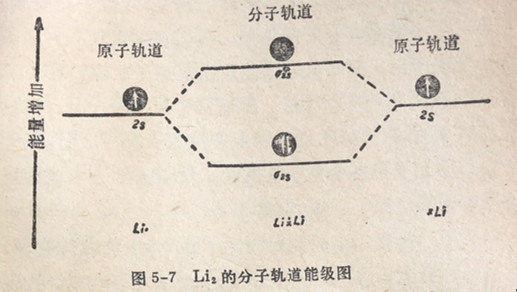
由于两个电子将都占据在能量较低的o2s成键轨道中,应该可能形成Li2。事实上,在温度靠近锂沸点的锂蒸气中存在着不小浓度的Li2分子。
在另一方面,可以估计到铍的双原子分子Be2不会是特别稳定的,因为四个价电子中的两个将占入o。成键轨道,另外两
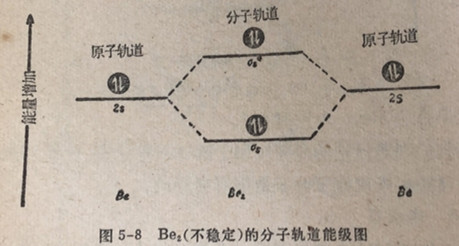
个价电子将被迫占入反键轨道。与氨的情况一样,能量的净净变化基本上是零,表明铍原子没有结合成双原子铍分子的明显倾向,这同实验结果是一致的,现在还不知道有稳定的Be2分子。