





我们已经了解了共价键是原子之间共用电子对,成键的两个原子各提供了相等数目的电子。当成键的两个原子中只有有二一个原子为电子对键提供了2个电子时,所形成的键叫做配位共价键。铵离子NH4+为配位共价键提供了一个实例。氨分子本身的三个键都是共价键的类型。氨分子容易同一个氢离子结合生成铵离子,表明原来属于氮原子的未共用电子对能够用于价键形成。
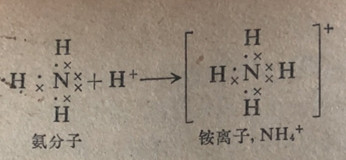
由于NH3是一个电中性分子,同一个氢离子相结合就给形成的铁铁离子带来了一个单位正电荷。同样,水分子同氢离子结合生成水合氢离子。
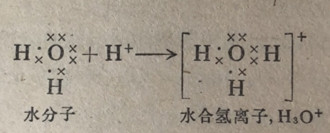
尽管在H3O+离子上还有一对电子可用于成键,但带正电荷的水合氢离子似乎已不再能吸引第二个氢离子(带正电荷)了。只有在下述情况下才有可能生成配位共价键:一个原子或离子在它的价电子层中有一对未共用电子对,和另一个原子或离子需要一对电子以便能达成较稳定的电子结构。配位共价键和正常共价键之间的主要区别在于它们的形成方式。一经形成之后,它们是没有区别的。
在我们对化学键的讨论中,我们一直认为电子是定域在成键原子的原子轨道之中。事实上,价电子是在以分子作为整体的所谓分子轨道中运动的,而不是限制在规定的个别原子的原子轨道中运动。在下一章里,我们将讨论到原子轨道是怎样结合起来形成分子轨道的的,并也将指出一些方式方法以表明这个概念对于说明分子的性质是特别有用的。
相关文章
共价键的类型https://www.999gou.cn/article.php?id=690
配位共价键是什么https://www.999gou.cn/article.php?id=333
离子键和共价键的提出和几种其他类型的微粒间的相互作用https://www.999gou.cn/article.php?id=2946
化学键中的共价键https://www.999gou.cn/article.php?id=1650
共价键的形成与价键理论要点https://www.999gou.cn/article.php?id=688
不同原子间的共价键有哪些https://www.999gou.cn/article.php?id=330
共价键的性质https://www.999gou.cn/article.php?id=4602