



















铵盐是氨眼酸化合的生成物,可由氨水跟酸中和制得这在上节已经讲过.从铵盐的分子组成来看,它是一类由铵离子(NH4+)和酸根离子结合而成的离子化合物,具有典型盐类的一切通性,现介绍如下:
.jpg)
铵盐的物理性质 铵盐都是晶体,在外观上它们与钠、钾相对应的盐很相象.例如,氯化铵就很象氯化钠,一切铵盐也都能溶解于水。
铵盐的化学性质
1.铵盐眼其他盐类和酸类类的反应铵盐和一般盐的性质一样,在水溶液里能眼其他盐类或酸类发生复分解反应。例如:
NH4C1+AGNO3=Agc1↓+NH4NO3
2NH4NO3+H2SO4(浓)=加热=(NH4)2SO4+2HNO3↑
2.铵盐睍碱类的反应铵盐跟碱的反应不同于一般的盐,情况比较特殊.铵盐跟碱反应时,就生成氢氧化铵和另一种盐,我们知道,盐眼碱起复分解反应生成新盐和新碱.如如以硫酸铵(铵盐)跟氢氧化钠(碱)反应,按理应生成氢氧化铵(碱)和硫酸钠(盐):
(NH4)2S04+2naoh=2NH4OH+NA2SO4
但由于NH4OH的分解解,实际上的反应却是
(NH4)2SO4+ 2NAOH=Na2SO4+2H2O+2NH3↑
这个反应的实质,可用简化离子方程式表示如下
NH4++OH<=> NH4OH
→NH3↑+H2O
铵盐与碱反应放出氨这个性质,是一切铵盐的通性,在实验室里就是利用这样的反应来制取氨的。
在实验室里检验铵盐的存在,也常利用这个性质,把要检验的盐(固体或溶液)放在试管里,滴入碱溶液(常用10%的氢氧化钠溶液),然后微微加热.如果闻到有刺激性的氨的气味;或者用润湿的红色石蕊试纸接近管口时变成了蓝色,那末就可断定被检验的盐盐一定是铵盐。
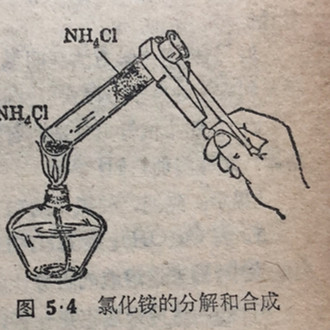 3.铵盐加热分解 铵盐的另一特性是加热容易分解.例它就会分解,生成易挥发的氯EC如,把氯化铵放在试管里加热,化氢和氨,但这二种物质在试管上部内壁遇冷时,又重新结合成氯化铵(图5·4).反应可用下式表示:
3.铵盐加热分解 铵盐的另一特性是加热容易分解.例它就会分解,生成易挥发的氯EC如,把氯化铵放在试管里加热,化氢和氨,但这二种物质在试管上部内壁遇冷时,又重新结合成氯化铵(图5·4).反应可用下式表示:
NH4C1=加热 受冷=NH3+HC1
此外,象硫酸铵、硝酸铵、磷酸铵等加热时,也都很容易分解.特别如碳酸铵[(NH4)2CO3]更容易分解,稍稍加热,就生成氨和碳酸,碳酸不稳定,又立刻分解生成水和二氧化碳:
(NH4)2C03=加热=2NH3↑+ H2CO3
→H20+CO2↑
铵盐的用途 铵盐在工业、农业以及日常生活上都有十分重要的用途.象硝酸铵和硫酸铵大量地用作肥料,硝酸铵还用来制造炸药,氯化铵可用作制干电池的原料.在焊接金属时,可用氯化铵来清除金属表面上的一层金属氧化物、因为当氯化铵接触到红热的金属表面时,会分解生成氯化氢,它立即跟金属氧化物反应,变成易溶的或挥发性的氯化物、这样,金属表面的氧化物就被去除,使焊料与焊件能更好地结
合。