Nitric acid(硝镪水)
分子式:HNO3
分子量:63.01
1.生产方法
(1)合成法:以氨为原料,使与空气混合,氨被氧化生成一氧化氮(NO),再继续氧化为二氧化氮(NO2),最后与水作用而成硝酸。
(2)分解法:用硝酸钠与浓硫酸共热得硝酸蒸气。
2 NANO3+H2SO4→Na2S04+ 2 HNO3
然后导入接受器中,将其凝缩为液体。
2.用途 为强氧化剂,用于组件及喷丝板清洗。工业上用途极广,可供制氮肥、硝酸盐、王水、硝化纤维素及炸药等。
3.质量指标 国家标准GB337-64(适用于浓缩稀硝酸法及直接合成法所制得的浓硝酸)
| 指标名称 | 单位 | 指标 | |
| 一级品 | 二级品 | ||
| 硝酸(HNO3)含量 | % | ≥98 | ≥97 |
| 硫酸(H2SO4)含量 | % | ≤0.08 | ≤0.12 |
| 氮的氧化物(N204)含量 | % | ≤0.3 | ≤0.4 |
| 灼烧残渣 | % | ≤0.3 | ≤0.05 |
注:①直接合成法制得的硝酸中无硫酸,故硫酸含量不检验。
②如硝酸与硫酸用作混酸,硫酸含量可不作检验。
③用户对质量(重金属)有特殊要求,可向生产厂订购直接合成法制得的硝酸。
4.物理化学性能 纯硝酸为无色液体,具有特殊臭味,一般带有微黄色,发烟硝酸是红褐色液体。
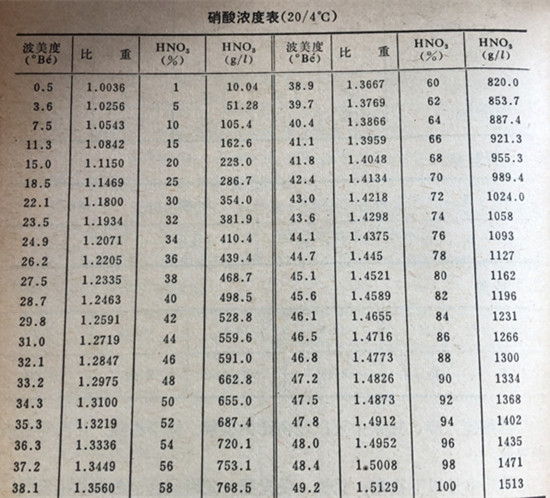
比重(25/4°):1.5027
熔点:-42C
沸点:83C
粘度:
| 温度(℃)/粘度(CPS)/浓度(%) | 40.0 | 50.0 | 70.0 | 90.0 | 100.0 |
| 20 | 1.56 | 1.82 | 20.03 | 1.35 | 0.89 |
| 40 | 1.68 | 1.91 | 2.06 | 1.48 | 1.04 |
折射率:
| 浓度(%) | 4.762 | 64.82 | 98.67 |
|
折射率 |
1.339 | 1.403 | 1.397 |
比热:
| 浓度(%) | 40.0 | 70.0 | 90.33 | 98.15 |
| 比热 | 0.669 | 0.610 | 0.53 | 0.475 |
溶解度:冷、热水中可以任何比例溶解。溶于乙醚。在乙醇中剧烈分解。
硝酸本身很不稳定,受热、受光照一定时间会分解而放出氧气。浓硝酸分解时生成二氧化氮(NO2),稀硝酸分解时生成一氧化氮(NO),越浓的硝酸越容易分解。
4 HNO3(浓)→ 2H20+4 NO2+O2
4 HNO3 (稀) → 2H2O+4 NO+3 02
硝酸为五价氮的含氧酸,是强氧化剂。能使铁钝化而不致继续被腐蚀。浓硝酸和稀硝酸都能与金属铜起作用,生成硝酸铜而使铜溶解。
浓硝酸腐蚀性极大,纸、布、皮肤等有机物接触到即腐烂,遇空气则发烟而有锐利闷室的臭味。硝酸氧化力强,能损害人体皮肤、粘膜、呼吸道。
5.包装及贮运 属一级无机酸性腐蚀物品。危规号91002。
可用罐车装运。可装于良好的耐酸坛、陶瓷坛、塑米料桶、玻璃瓶中,严密封口再装入坚固木箱、铁桶或半透笼木箱,箱内用不燃材料衬垫。坛或塑料甬装每箱净重不超过50kg。瓶装不超过30kg。