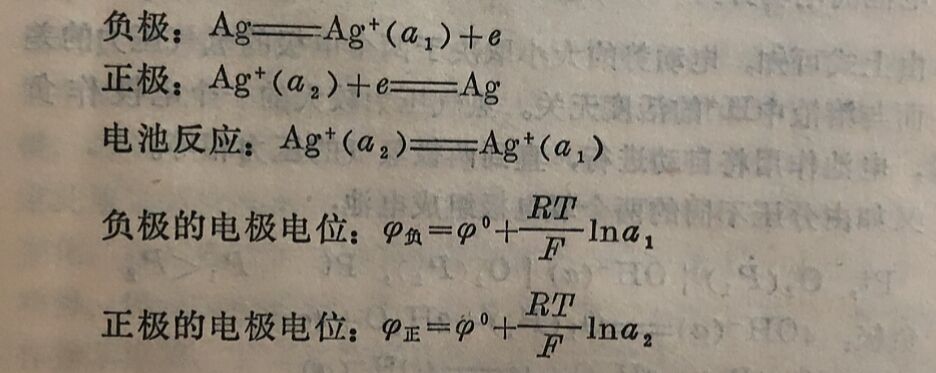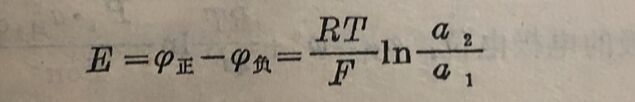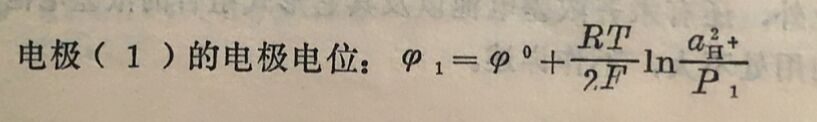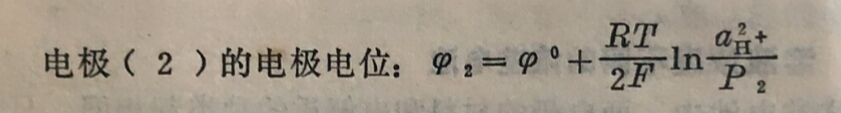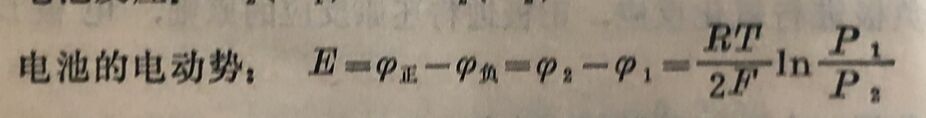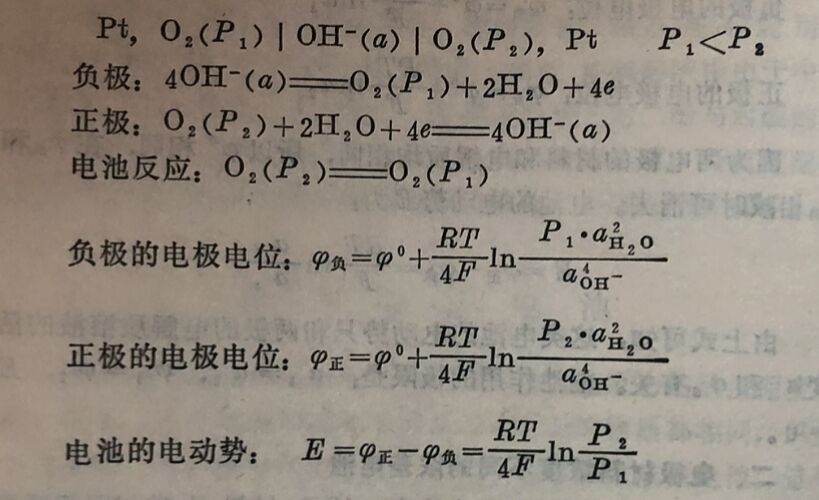浓差电池
铜臭 / 2022-07-23
能斯脱公式指出电极电位是随氧化态和还原态的活度而变化的。那末,两个电极即使其氧化态和还原态的物质都相同,只是活度不同,它们的电极电位也不相同,也可以组成原电池。这种由两个组成相同、但活度(或浓度)不同的电极组成的原电池,叫作浓差电池。浓差电池的电池作用仅仅是一种物质从高浓度状态向低浓度状态转移。当浓度相等时,电动势等于零,这时电池作用达到极限,不能再进行。浓差电池主要有两类:溶液浓差和电极材料浓差,分别叙述如下:
一、溶液浓度不同的浓差电池
在这类电池中,两电极的材料和电解质的种类都相同,只是 电解质溶液的浓度不同。例如有两个电极: AgIAgNO₃(a₁),AgIAgNO₃(a₂),且a₂>a₁。 根据能斯脱公式可知,φ₂>φ₁。两电极组成电池时,离子活度小的电极必为负极,离子活度大的电极必为正极。电极电池:
AglAgNO₃(a₁)IAgNO₃(a₂)IAg a₁<a₂
根据负极进行氧化反应,正极进行还原反应的原则,电极反应为:
因为两电极的材料和电解质均相同,所以φ⁰相同,在φ正和φ负相减时可消去。电池的电动势E为:
由上式可知,这类电池的电动势只和两极的电解质溶液的活 度a₁和a₂有关。电池作用的极限是: a₁=a₂, φ₁=φ₂, E=0。
二、电极材料浓度不同的浓差电池
这种浓差电池是在同一溶液中,插入材料种类相同但活度(或浓度)不同的两个电极所构成。例如有分压不同的两个氢电 极: (1)Pt, H₂(P₁)|H⁺(a), (2)Pt, H₂(P₂)|H⁺(a),P₁>P₂。则:
由于P₁>P₂,故φ₂>φ₁因此电极(1)为负极,电极(2)为正极。组成的原电池为:
Pt,H₂(P₁)|H⁺(a)|H₂(P₂), Pt
负极: H₂(P₁)= =2H⁺(a)+2e
正极: 2H⁺(a)+2e=H₂(P₂)
电池反应: H₂(P₁)=H₂(P₂)
由上式可知,电动势的大小取决于两个电极的氢气压力的差别, 而与溶液中H⁺的活度无关。氢气压力较大的一个电极作负极时,电池作用将自动进行,直到两极氢气的压力相等。
又如由分压不同的两个氧电极组成电池:
以上说明,由两个氧电极组成的电池中,当氧气压力较大的一个电极作正极时,电池作用将自动进行,直至两极氧气压力相等。
此外,还有汞齐浓差电池以及其它形式组合的浓差电池,因对我们用处不大,不作详述。