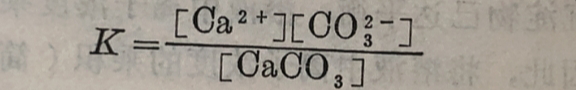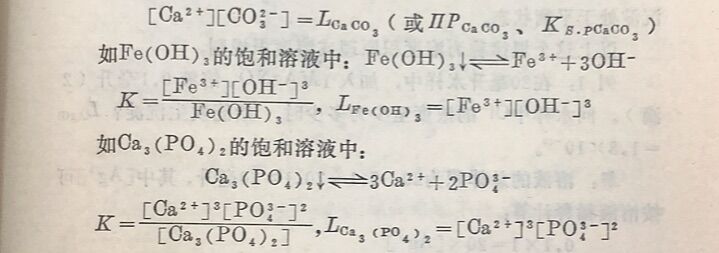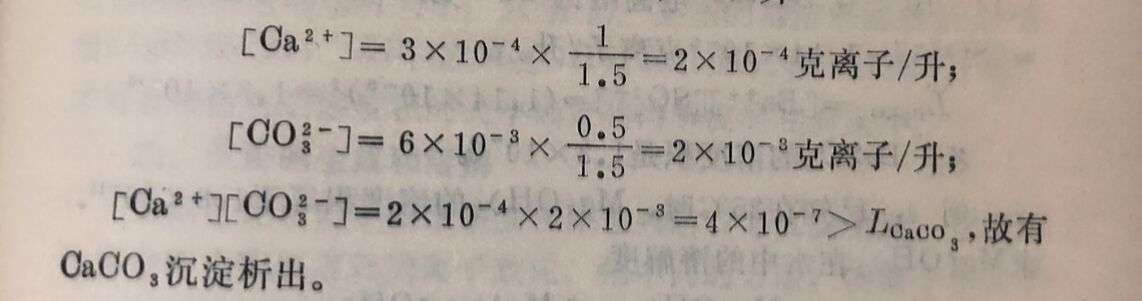多相离子平衡一沉淀和溶解
铜臭 / 2022-07-21
前面讨论的是弱电解质的电离平衡,是均匀液相中的平衡,称为单相(或均相)平衡。本节将讨论有关难溶电解质的沉淀与溶解的平衡,这个在固相和液相之间形成的平衡,称为多相(或异相)平衡。
沉淀和溶解,在水处理和化学实验工作中是经常碰到的现象。例如,把天然水中的杂质(如Ca²⁺和Mg²⁺)转变成难溶的沉淀物予以除去;锅炉受热面结垢与汽轮机叶片上积盐以及使其溶解除掉;水中一些杂质的测定和分离等,都要利用有关沉淀和溶解的理论。
物质能否生成沉淀或能否溶解,可利用溶度积进行判断。
溶度积和溶度积原理
1.溶度积。任何一种难溶电解质,都不是绝对不溶的。所以水中若有难溶物质存在时,就成为该物质的饱和溶液。虽然此溶液很稀,但仍存在着固体和溶液中离子之间的多相平衡,如在CaCO₃的饱和溶液中:
根据质量作用定律,可以写出这个反应的平衡常数表达式:
由于化学上规定把纯固体物质的浓度作为1,所以上式可写 为: K=[Ca²⁺][CO₃²⁻]。 为了表达这个常数的特殊性,常以L、IIP、Ks.p等符号来代替K,并将难溶电解质的化学式注在右下角。因而上式可写成:
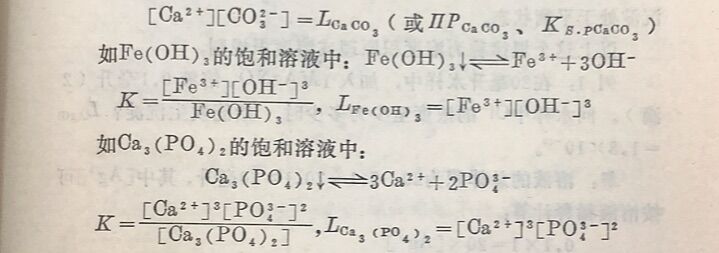
由此可知,在一定温度下难溶电解质的电离方程式中的离子系数都等于1时,此难溶电解质各种离子浓度的乘积是一个常 数。如CaCO₃电离方 程式中Ca²⁺和CO₃²⁻的系数都是1,则Lcaco₃=[Ca²⁺][CO₃²⁻]。若电离方程式中离子系数不都等于1时,此难溶电解质各离子浓度方次数(方次数等于电离方程式中各离子相应的系数)的乘积是一常数。如Ca₃(PO₄)₂电离方程式中Ca²⁺ 的系数为3 ,PO₄³⁻的系数为2,则Lca₃(PO₄)₂ =[Ca²⁺]³[PO₄³⁻]²。这一常数称为难溶电解质的溶度积常数,简称溶度积。
由于物质的溶解度随温度而改变,因此,温度改变时,溶度积也随之改变。故在应用溶度积具体的数值时,必须注意温度。
2.溶度积原理。必须指出,溶度积是溶液中各离子浓度乘积的极限值,是沉淀物与溶液达平衡的标志。离子浓度乘积小于落度积时,说明溶液与沉淀物尚未达平衡,溶液中不会有沉淀物析出,溶液中的离子可以在其乘积小于溶度积的浓度范围内,以任意的浓度存在。但只要溶液中有沉淀物存在,不论其量多少,就表明溶液与沉淀物已达平衡,溶液中离子浓度乘积必等于沉淀物的溶度积。因此,将溶液中离子浓度的乘积(简称离子积)和溶度积比较,判断有无沉淀生成:
离子积<溶度积,溶液未达平衡,无沉淀析出。
离子积=溶度积,溶液达饱和,但仍无沉淀析出。
离子积>溶度积,有沉淀析出直至离子积=溶度积,溶液与沉淀处于平衡状态。
以上这个规律称为溶度积原理或溶度积规则。
例1:在20毫升水样中,加入1MAgNO₃溶液0.1毫升(2滴)。问水样中CI⁻的浓度至少为多少时,始能发生沉淀? Lagcl =1.8×10⁻¹⁰。
例2:某生水含有Ca²⁺3x10⁻⁴克离子/升。在此一升生水中加入0.5升6×10⁻³M的Na₂CO₃溶液时,问是否有沉淀产生?沉淀完毕后,溶液中[Ca²⁺] 为多少?已知Lcaco₃=4.8X10⁻⁹(不考虑CaCO₃的水解)。
解:混合后总体积为: 1升+0.5升=1.5升
沉淀完毕后,仍维持下列平衡:
CaCO₃⇔Ca²⁺+CO₃²⁻
设达平衡时,饱和溶液中[Ca²⁺]= x
已沉淀的[Ca²⁺]=2x10⁻⁴-x
因为生成CaCO₃沉淀时,一个Ca²⁺要与1个CO₃²⁻结合。 故已沉淀的[CO₃²⁻]=已沉淀的[Ca²⁺]=2×10⁻⁴-x。
则溶液中[CO₃²⁻]=2×10⁻³-(2x10⁻⁴-x)
=1.8×10⁻³+x
[Ca²⁺][CO₃²⁻]=x(1.8x10⁻³+x)= Lcaco₃=4.8X10⁻⁹
因与1.8X10⁻³比较x很小,可以略而不计,则1.8x10⁻³+x≈1.8×10⁻³
x×1.8×10⁻³=4.8×10⁻⁹
x=2.7×10⁻⁶克离子/升
答:沉淀完毕后,溶液中的[Ca²⁺]=2.7X10⁻⁶克离子/升。







![硫酸亚铁铵标准溶液c[(NH4)2Fe(SO4)2]厂家价格](images/202207/thumb_img/1630_thumb_G_1658535105210.jpg)








![硫酸铈标准溶液浓度 c[Ce(SO4)2] = 0.1500 mol/L价格](images/202207/thumb_img/1632_thumb_G_1656925752112.jpg)



![硝酸铜标准溶液 c[Cu(NO3)2]= 0.01000 mol/L价格](images/202207/thumb_img/1653_thumb_G_1658537651764.jpg)