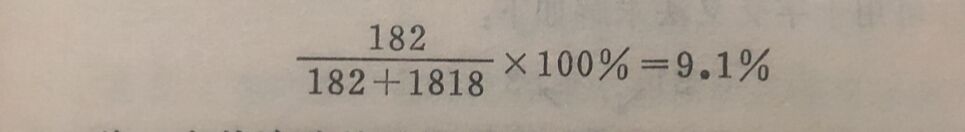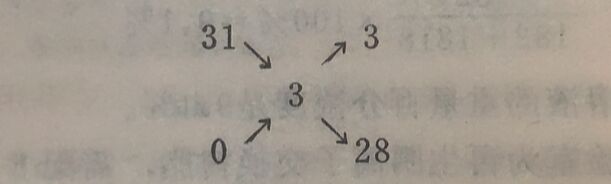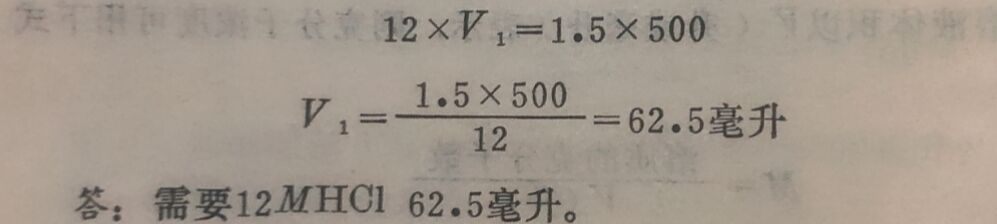例4:如何配制5%(重/容) AgNO₃溶液500毫升? 解:需要AgNO₃的重量: 500x0.05=25克
答:称取25克AgNO₃,先用少量水溶解,再用水稀释至500毫升即得。
由于物质溶解时,溶液的体积要发生变化,因此在配制时, 通常要放在已确定体积的容器——容量瓶——中稀释,这与配制重量百分浓度方法不同。由于溶液体积随温度而改变,因此溶液体积百分浓度会受到温度的一定影响。
二、克分子浓度
克分子浓度分重量克分子浓度和体积克分子浓度两种:
1.重量克分子浓度,以“m"表示。用1000克溶 剂中所含溶质的克分子数来表示的浓度,叫做该溶液的重量克分子浓度,以字母表示。例如,在1000克水中含有1克分子(即98克) H:SO,,则此溶液的重量克分子浓度为1m。
例5: 250克水中含有20克NaOH,计算此溶液的重量克分子浓度。
解: 1克分子NaOH重40克,则20克NaOH 的克分子数为:
20/40=0.5克分子
溶液重量克分子浓度为:0.5/250×1000=2m
答:此溶液的重量克分子浓度为2m。
2.体积克分子浓度,以“M"表示。用1升溶液中所含溶质的克分子数(或1毫升溶液中所含溶质的毫克分子数)来表示的浓度,叫做该溶液的体积克分子浓度(简称为克分子浓度), 以M表示。例如,1 升NaOH溶液里含有1克分子NaOH (即40克),则此溶液浓度就是1M;反之,2MNaOH溶液,则表示每升NaOH溶液中含有2克分子NaOH (即80克)。
若溶液体积以V(升或毫升)表示,则克分子浓度可用下式计算:
由此可见,如果溶质的克分子数不变,则溶液的克分子浓度和体积成反比。此式可用于溶液的稀释,如以M₁和V₁分别代表 浓溶液的克分子浓度和体积,M₂和V₂分别代表稀溶液的克分子浓度和体积,由于稀释前后溶质克分子(或毫克分子)数不变,可得溶液的稀释公式:
M₁V₁=M₂V₂
例6: 如何配制500毫升0.1MNaOH溶液?
解: 500毫升0.1MNaOH溶液中所含溶质的克分子数为:
0.1×500/1000=0.05克分子
因1克分子NaOH的重量是40克,0.05克分 子NaOH的重量为:
0.05X40=2克
答:“称取2克NaOH,先用少量水溶解,再用水稀释至500毫升即成。
例7:欲配制500毫升1.5MHCI溶液,问需要12MHCl多少毫升?
解:根据公式(6-4)M₁V₁=M₂V₂
设需要12MHC1毫升数为V₁,将已知数值代入上式得:








![硫酸亚铁铵标准溶液c[(NH4)2Fe(SO4)2]厂家价格](images/202207/thumb_img/1630_thumb_G_1658535105210.jpg)








![硫酸铈标准溶液浓度 c[Ce(SO4)2] = 0.1500 mol/L价格](images/202207/thumb_img/1632_thumb_G_1656925752112.jpg)



![硝酸铜标准溶液 c[Cu(NO3)2]= 0.01000 mol/L价格](images/202207/thumb_img/1653_thumb_G_1658537651764.jpg)