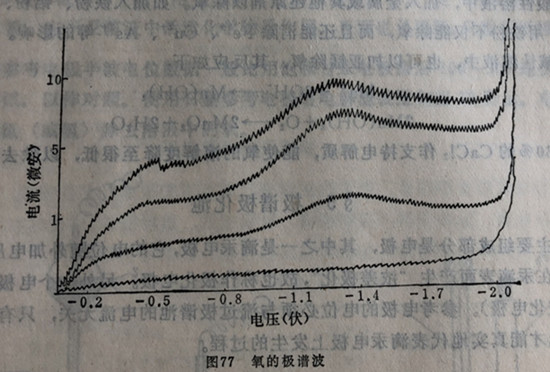
氧是极谱分析中干扰最大的因素之一。这是因为水溶液中溶解有少量的氧(在常温下氧的溶解度为8毫克/升),它能在滴汞电极上还原,因而出现两个波(如图77)。
氧的还原一般分为两步:第一步还原为过氧化氢,其反应如下:
O2+2H++2E→H2O2(酸性介质)
O2+2H2O+2E→H2O2+2OH-(中性或碱性介质)
第二步相当于过氧化氢还原为水或氢氧根:
H2O2+2H++2E→2H2O(酸性介质)
H2O2+2E=2OH-(碱性介质)
图77的第一个氧波的半波电位约在0.2伏特(对S·C·E)处;第二个氧波的半波电位约在-0.8~1,3伏特(对S・C·E)处。
氧波占了外加电位0,01.3伏特(对S・C・E)之间很大的范围。这个范围正是极谱分析最重要的区域。大多数的元素都在此区域出波,这样氧波势必遮盖其他波图,所以必须除氧。
除氧的方法有下列几种种:
1.在碱性溶液中,如被测物质及支持电解质与无水亚硫酸钠不起作用的,可使用亚硫酸钠除氧,一般般用量为1%,反应如下:
O2+2NA2SO3→2NA2SO4;
2H++2NA2SO3→SO2+H2O+2NA+。
由于在酸性溶液中产生的SO2在一0,37伏特处出现一个还原波,对极谱分析有影响,因而此法不适用。

2.通入惰性气体,使溶液表面气相中氧的分压降低而除氧。氮和氢可适用于不同pH的底液,CO2适用于酸性溶液,因为CO2能中和OH-,改变底液的plH。CO2的比重较大,除氧效果较好。使用惰性气体除氧时,要将惰性气体纯化后方能使用。氢及氮的纯化可通过以下顺序:
1)加入0.2N高锰酸钾;2)以10%焦性没食子酸及15%氢氧化钾混合溶液;3)用蒸馏水,洗涤。
CO2只需通过0.2N高锰酸钾溶液和蒸馏水洗涤就能使用。
3.在酸性溶液中,加入金属或其他还原剂以除氧。如加入铁粉、铝粉、硫酸亚铬、盐酸羟胺等。用铁粉不仅能除氧,而且还能消除Fe3+、Cu2+、As3+等的影响。
4.在碱性溶液中,也可以加亚锰除氧,其反应如下:
Mn2++20H-→Mn(OH)2
2MN(OH)2+O2→2MNO2+2H2O
5.以30%的CaC12作支持电解质,能使氧的溶解度降至很低,以除去氧的干扰。
编辑网站:https://www.999gou.cn 999化工商城