












已知络合滴定有下列的解离平衡
RX<=>R+X
C(1-a)Ca Ca
K不稳=Ca2/1-a
式(1)中C为络合物的原始浓度(理论值),a为络合物的解离度,即
已离解的质点数
a=————————
理论质点数
下面用“等克分子法”求a
[X]+[R]=总和(即克分子数或毫克分子数)
0 10 10
1 9 10
2 8 10
3 7 10
4 6 10
5 5 10
6 4 10
7 3 10
8 2 10
9 1 10
10 0 10
以(X〕和〔R)的比值为横坐标,以吸光度为纵坐标,根据〔X〕与〔R〕的比值测出相应的吸光度(消光值),作图得出实线所示的实验结果。
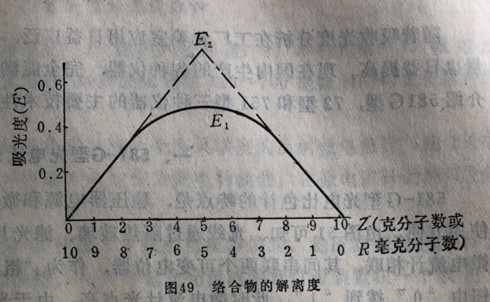 由图49可知,随着〔X〕由0→5(即R10→5),生成络合物的质点数是逐渐增加的,因此吸光度(消光)应呈直线上升。随着X)由5→10(R〕由5→0)生成络合物的质点数又逐渐减少,因此吸光度(消光)值应以直线下降。在〔X)〔RP)=5:5时,应该是络合最完全,即生成的质点数最
由图49可知,随着〔X〕由0→5(即R10→5),生成络合物的质点数是逐渐增加的,因此吸光度(消光)应呈直线上升。随着X)由5→10(R〕由5→0)生成络合物的质点数又逐渐减少,因此吸光度(消光)值应以直线下降。在〔X)〔RP)=5:5时,应该是络合最完全,即生成的质点数最
多。因此,吸光度(消光)应该是溶E2(理论值)。但是,由于络合物日光解离,使得吸光度(消光)曲线不,是∧形而是弧形,即使得(X〕:(R)=5:5时的吸光度(消光)不是E2而是E1。因此,
E2-E1/E2=已解离的质点数/理论质点数=a (2)
以(2)式代入(1)式得
Ca2 已解离的质点数 C(E2-E1)2
K不稳=———=————————=——————
1-a 1-E2-E1/E2 E2×E1
上式中C为实际配制的溶液浓度,E1为测得的吸光度(消光值),E2为实测得出へ线通过0和10的两切线在5:5纵轴上的交点。通过作图可得E2的数值。