熔点的测定
化学试剂,九料化工商城 / 2020-10-22
一、熔点的测定实验目的
1.学习熔点的测定方法;
2.学习加热及使用温度计的方法。
二、熔点的测定提要
物质的信点是在一定压力下该物质的固液两相蒸气压相等时的温度,也就是固相与液相共存时的温度。
固态纯物质(晶体)在一定压力下,加热到近熔点时,固液两相之间的变化非常灵敏,由开如熔融到全部熔融,温度变化一般不超过0.5~1℃。含有杂质的物质的熔点较纯物质的为低,而且熔融过程中温度的变化也较大,这一特征可作为鉴别物质纯度的一种依据。
三、仪器和药品
1.仪器
提勒管、毛细管(一端封闭)、温度计、表面皿、玻璃棒、铁架、铁夹、酒精灯、铁圈、石棉铁丝网、滤纸碎片、浓硫酸回收瓶、缺口的单孔软木塞
2.药品
硫酸H2SO4(浓)[注]
[注]对于熔点在220℃以下的样品,用浓硫酸作为加热介质较为适宜。除浓硫酸外,还可采用磷酸(可用于300℃以下)石蜡油或有机硅油等作为加热介质。
四、熔点的测定实验内容
取出许待测熔点的干燥样品(约0.1克萘),置于干净的表面皿上,用玻璃棒将它研成粉末。取1根毛细管(一端封闭),将其开口端向下插入粉末中,然后把毛细管开口端转向上,轻轻地在桌面上敲击;如此往复数次,使管内样品达2~3mm高为止。拭去管外沾附着的样品粉末。按同样操作再装好1根毛细管。将2根已装好样品的毛细管放在表面皿上待用。
2.熔点的测定
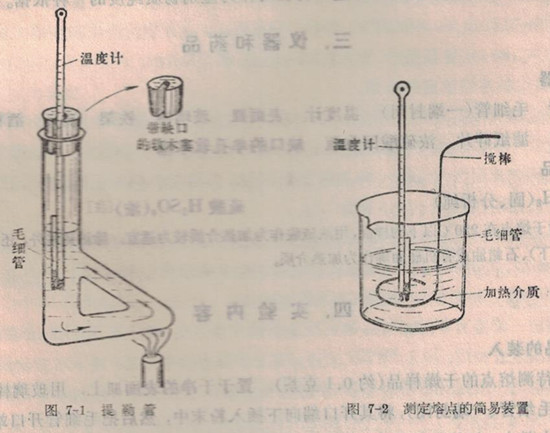
将提勒管[注1](又称b形管)垂直夹在铁架上,在管口配有缺口的单孔软木塞;插入已校正过的温度计,温度计的刻度应面向软塞缺口,调节温度计的水银球位置使在提勒管上下两叉管口之间(图7-1)。取出软木塞及温度计,小心加入浓硫酸(用作加热介质),至高度超过上叉管口即可。把装好样品的毛细管借少许加热介质粘附于温度计下端[注2](图7-1),然后将温度计缓慢地插入提勒管中。
在提勒管的弯曲支管底部缓缓加热,开始时升温速度可较快,约每分钟上升5℃,到距离熔点10~15℃时,调整火焰使每分钟上升约1~2℃(可垫以石棉铁丝网,必要时可将酒精灯移开一下),越接近熔点,升温速度应越慢。控制好升温速度是测准熔点的关键。
记录样品开始低陷并有液相产生(初熔)的温度计读数和固体完全消失(全熔)时的温度计读数。
待浓硫酸冷却至熔点以下30℃左右,另取一根已装好样品的毛细管,重复以上操作,并取
每次熔点测毕,将温度计取出(注意切勿将浓硫酸滴溅在实验桌或衣物等上),待其冷却后,用滤纸碎片擦去附着于其表面的硫酸,再用水冲洗之。待提勒管中的浓硫酸冷却后,倒入回收瓶中(若经指导教师同意,亦可倒回原瓶中)。
[注1]亦可用其它仪器装置(如图7-2所示)进行熔点的测定。
[注2]亦可用乳胶管细圈把毛细管固定在温度计上。
[注3]如果要测定未知物的熔点,应先对样品粗测一次,加热可以稍快。知道大致的熔点范围后,待加热介质的温度降至熔点以下约30℃左右,再另取装好样品的毛细管进行精确测定。
五、熔点的测定实验前准备的思考题
(1)纯物质(晶体)为什么有固定的熔点?
宝帕点欲
(2)用浓硫酸作加热介质,在操作过程中有哪些应注意之处?
(3)当加热到接近熔点温度时,加热速度为什么一定要慢?