



























正象电离势是从原子取走一个电子形成正离子所需要的能量的衡量尺度一样,另一个数量电子亲合势是给一个原子加入
一个外来电子形成负离子时所释放的能量种衡量尺度。这个变化可以用下式表示:
x+e-→X-+能量
金属原子得到电子形成负离子的倾向极小,因此它们的电子亲合勢是很小的(表7-9)。在另一方面,非金属元素有大的电子亲合勢,因为它们容易加合电子,并且是好的氧化剂。
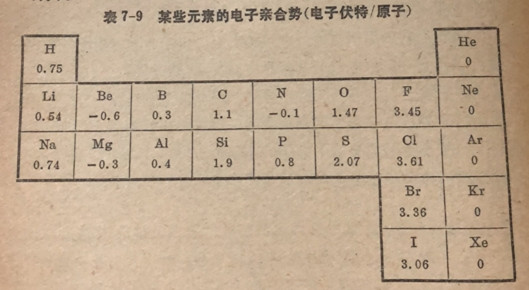
一般而言,在周期表沿着周期自左向右,元素依次有较高的电子亲合势并且非金属性增强。不过在第二周期中,人们可以注意到铍(28亚层全充满)氮(2p亚层半充满)和氖(所有亚层全充满)是例外,在这些情况全充满和半充满都代表稳定结构。