











我们是从参加成键的电子主要定域在成键原子的原子轨道之中的观点来考虑价键形成的。在分子轨道理论中,假
定成键原子的原子轨道组合在一起形成了分子轨道,在分子軌轨道中电子围绕整个分子而运动。
分子轨道理论处理电子在分子中的分布和在原子中处理电子在原子轨道中的分布方式是极为相似的。
分子轨道理论假定在分子中诸原子核的周围存在着分子轨道。这些分子轨道是在分子中最可能找到给定电子的区域。不认为价电子是定域在各个原子之内,而是认为价电子是围绕着整个分子而运动的。
分子轨道与组成分子的原子的原子轨道相类似。事实上,把原子轨道作适当的组合就可以近似地求出分子轨道的形状。
两个原子轨道组合起来形成两个分子轨道。其中的一个分子轨道是由原子轨道重叠部分相减而产生的,叫做反键轨道。另个分子轨道是由原子轨道重叠部分相加而产生的,叫做成键轨道。
由两个原子轨道组合所形成的两个分子轨道中,成键轨道的能量比反键轨道的能量低。因此,电子倾向于优先充填到能量比、较低的成键分子轨道中,其次才充填到能量较高的反键分子轨道中,正像电子倾向于充填到能量较低的原子轨道中、然后才充填到能量较高的原子轨道中的情况一样。
有如我们在第三章(第3.2节)已看到的,8原子轨道的形状被认为是球状的。分子轨道理论设定一个原子的8轨道与另一个原子的s轨道组合在一起形成两个分子轨道(图5-1),8原子轨道的这种组合体叫做o(读音西格玛)分子轨道。应该注意的是,重叠相加所产生的成键分子轨道的能量比组合成分子轨道的任何一个原子轨道的能量都低。重叠相减所组合的反键轨道的能量比两个原子轨道中的任何一个能量都高。有如我们可以预期的,电子倾向于占人能量比较低的成键轨道。这是因为一个给定的电子在成键轨道中将同时被两个核所吸引,而在反键轨道或两个原子轨道中给定的电子将主要只被一个核所吸引。注意在图5-1中反键轨道未能包括两个核之间的某些空间。
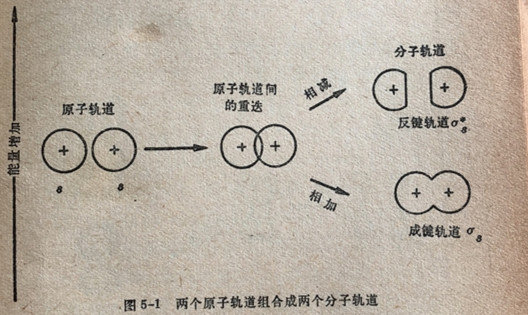
反键轨道的符号往往带一个是号号“*”,以便和相对应的成键轨道相区别。常用一个下脚字母来标志组成分子轨道的原子轨道的类型。举例来说,由两个s原子轨道组合成的成键分子轨道和反键分子轨道分别用符号 os。和os*“来标志,有如图5-1所示。通常把它们叫做“西格玛s”和“西格玛s星号”。
两个p原子轨道可以有两种组合方式一即头碰头或肩并肩相结合一产生两个分子轨道(图5-2)。当两个原子的p原子轨道头碰头相结合时,得到的的两个分子轨道叫叫σ轨道,和s原子轨道的情形一样。不过当两个P轨道肩并肩地相组合时,得到的分子轨道叫做(读音:派)轨道。
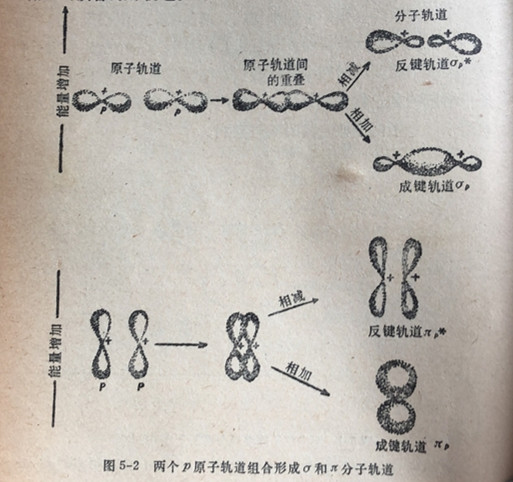
每个原子含有3个P原子轨道-px,py和pz(参见第3.20节)。其中的一个(例如px)头碰头地与另一个原子的相应P原子
轨道相组合形成两个o分子轨道σpx和O*px 另外两个P原子轨道py和pz各与另一原子的相应P原子轨道肩并肩地相结合,产生两个π分子轨道。这两套分子轨道彼此以接近直角的方向而取向,如果一套分子轨道在一套坐标轴中中沿着y轴而取向,另一套则沿着2-轴而取向。符号π py和π pz(通常叫做“π-p-y”和“π-p-z”)对应于成键轨道,而π*py,和π *pz,(叫“π-p-y星号”和“π-p-z星号)则对应于反键轨道。除了它们的方向外,πpy和πpz是相同的并有相同的能量。
这样一来,在两个原子中的六个2原子轨道组合起来总共形成六个分子轨道。如果认为op和o*p轨道是沿着x轴的,那么两
套πp和π*p轨道分别是沿着y-轴和z-轴而取向的,这六个分子轨道是opx和o*px、πpy和π*py,以及πpz和π*pz。