铀在化合物中可以以3、4、5、6价等不同价态存在,以4价和6价化合物最为重要.六价的铀一般常以铀酰根(UO22+)形式存在,pH~4时则生成UO2(OH)2沉淀析出,六价铀具有两性,在氢氧化钠溶液中则生成铀酸盐Na2UO4及重铀酸盐Na2U2O7.四价铀的化学性质相似于钍,U(OH)4不具两性,在空气中氧的缓慢氧化下四价铀能变成六价,倘有铁(Ⅲ)及其他氧化剂存在下则迅速氧化成六价.铀的比色测定方法大多数是以铀酰离子的显色反应为根据的,部分方法则是利用铀(Ⅳ)的显色反应(如偶氮胂Ⅲ)而拟定的.在通常应用的比色方法中,偶氮胂Ⅲ法具有很高的灵敏度和选择性,应用已比较普通.此外用来测定铀的试剂还有偶氮胂Ⅱ和Ⅲ、偶氮氯膦Ⅰ、偶氮氯膦Ⅲ等胂羧基和膦羧基偶氮化合物.
.jpg)
乙二醛双[2-羟基缩苯胺](GBHA)在前面已介绍用于钙的测定,但它在碱性溶液中与UO22+的反应也可用于光度测定铀,它们之间形成红紫色的络合物:
虽然这一反应选择性不高,许多其他的二价阳离子皆有类似反应,但是GBHA-UO2的络合物不被EDTA所破坏,以EDTA为掩蔽剂可使反应具有良好的选择性,该反应的适宜条件是在酒石酸盐存在下pH12.5~13的水-甲醇(1:1)介质中.
新近提出的2-[(5-溴-2-吡啶)偶氮]-5-二乙氨基苯酚(简称5-Br-DEPAP,有些文献中也简称Br-PADAP)是测定铀的一种良好的显色试剂:
试剂能与过渡金属发生灵敏的颜色反应.它与铀的反应灵敏度为PAR的两倍,而且选择性更好,以TOPO萃取直接在有机相中显色,对铀(Ⅵ)的测定几乎是特效的.5-Br-DEPAP与U(Ⅵ)的反应最适pH为4.1,此时形成组成比为1:1的络合物,在554和586毫微米处有两个吸收峰,摩尔吸系数分别为ε554=4.65×104和ε586=5.63×104.当pH增高时,该络合物发生分解,但在NaF存在下,于pH6-8能形成稳定的含氟三元络合物,在最适pH7.3时,其络合物的摩尔吸收系数为ε542=5.51×104和ε578=7.32×104.该络合物的结构被描述为:
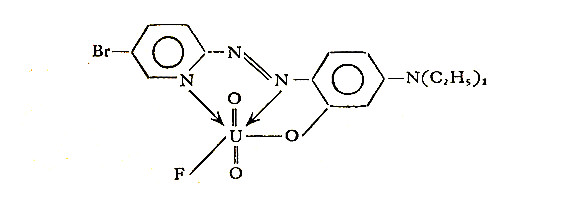
三元络合物能为许多有机溶剂所萃取,适于铀的测定,已拟定过矿石中铀的测定方法.
偶氮胂Ⅰ的结构式为:在弱碱性介质(pH7.5-9.0)中试剂与铀酰离子形成蓝色络合物,而在此溶液中试剂呈政瑰红色,其吸收光谱曲线如图Ⅷ-35.在pH8.5时,UO22+离子与偶氮胂Ⅰ络合物的吸收峰位于596毫微米处,λ=596毫微米时其摩尔吸收系数等于2.3×104.
在弱碱性溶液中,偶氮胂Ⅰ与多种金属离子呈显色反应,常加入EDTA来掩蔽Al、Bi、Co、Cu、Fe、Ni、Pb和Zn等金属的离子;酒石酸盐掩蔽Ti.由于EDTA大量存在时能引起偶氮胂Ⅰ铀酰络合物颜色变浅,因此在制作标准曲线时必须在相同条件下进行以消除误差.此外,钍的存在将干扰铀的测定,通常须预先将它分离除去.
试剂和溶液:
1.偶氮胂Ⅰ 0.05溶液,50毫克试剂溶于100毫升水中;2.铀(Ⅵ)标准溶液 含铀1毫克/毫升.称取2.1080克UO2(NO3)2·6H2O溶解于适量水中,加入1毫升浓硝酸后继续加水至1升,溶液浓度可用重量法进行校正.制作标准曲线时根据需要用0.01N HNO3进行稀释;3.pH8.6缓冲溶液 溶解2克硼酸和2克氯化钾于适量水中,加入6.5毫升1N NaOH溶液,用水稀释至500毫升.
测定步骤:取含铀(Ⅵ)量不大于300微克的分析试液一份,除去干扰离子后移入50毫升容量瓶中,检查pH使之在3-5之间,加入4毫升偶氮胂Ⅰ溶液,小心摇匀,加入10毫升缓冲溶液,加水稀释至刻度,摇匀后在596毫微米处测量吸光度,以空白溶液为对照.