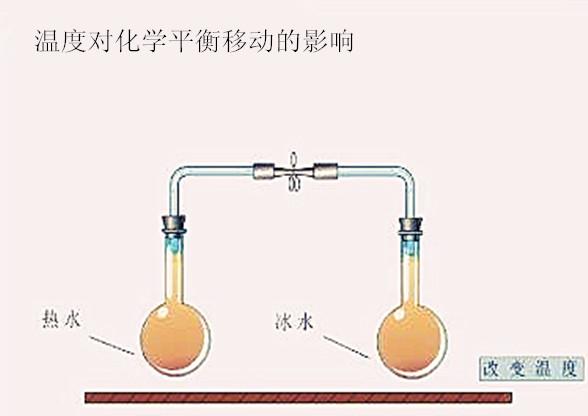
温度对化学平衡的影响与浓度和压力的影响不同,温度改变将导致Kθ值发生变化,从而使平衡发生移动。
根据式△Gθ=△Hθ-T△Sθ和式△Gθ=-RTlnKθ=-2.303RTlgKθ(前面文章中提到),得到
lnKθ=(-△Hθ/RT)+△Sθ/R (1-28)
设某一可逆反应在温度T1时的平衡常数为Kθ1,温度为T2时的平衡常数为Kθ2,△Hθ和△Sθ在温度变化不大时可视为常数。则
lnKθ1=(-△Hθ/RT1)+△Sθ/R
lnKθ2=(-△Hθ/RT2)+△Sθ/R
两式相减,得
ln(Kθ2/Kθ1)=(△Hθ/R)(T2-T1)/T1T2 (1-29)
式(1-29)表明了温度对平衡常数的影响:对于放热反应,△Hθ<0,温度升高(T2>T1),则Kθ2<Kθ1,平衡逆向移动。降低温度则相反。对于吸热反应,△Hθ>0,温度升高,平衡向正方向移动。降低温度将相反。总之系统温度升高,平衡向吸热反应方向移动;系统温度降低,平衡向放热反应方向移动。
例1-23 已知反应CO2(g)+H2(g)⇌ CO(g)+H2O(g),在973K时Kθ1=0.62,在1073K时Kθ2=0.91,通过计算说明此反应是放热反应还是是吸热反应。
解:根据(1-29)式得到
ln(0.91/0.62)=(△Hθ/8.314)(1073-973)/1073×973
△Hθ=33.3kJ/mol>0
因此是吸热反应。