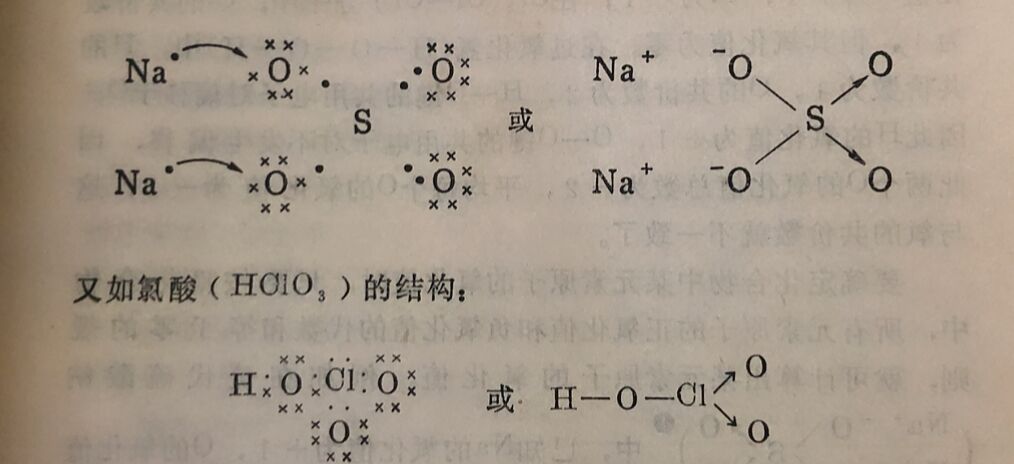二、氧化值
从电子的得失或偏移的角度出发,引入元素氧化值(或氧化数)的概念。氧化值是由原子得失的电子数来决定的:失电子时,氧化值为正;得电子时,氧化值为负。
对于形成离子键的元素来说,由于离子键的形成过程也就是原子得失电子的过程,因此离子的电荷数也就等于元素的氧化值。例如NaCl中Na的氧化值是+1, CI的氧化值是-1,即与离子的价数是一致的。
对于形成共价键或配位键的元素来说,虽然电子对是共用的,没有电子的得失,但可以假定当共价键断裂时,共用电子对完全转移到非金属性强(或电负性大)的元素一边,这时每个原子所失去或得到的电子数就是该元素的正、负氧化值。例如在CO₂中,C和O原子间的共用电子对偏向于非金属性强的O原子,它们之间的共价键断裂时,可认为共用电子对完全转移给O原 子,故C的氧化值为+ 4, 2个O原子各得到2个电子,故O的氧化值均为-2。但是当两个相同原子间的共价键断裂时,共用电子平均地分配给两个原子,因此,单质中元素的氧化值为零。例如H₂(H:H)分子中H的氧化值为零。由此可见,共价数不 一定等于氧化值。又如在HCl中, H和Cl的共价数各为1,其氧化值日为+1, Cl为-1;在C1₂(Cl—Cl)分子中,Cl的共价数为1,但其氧化值为零。在过氧化氢(H一O一O一H)中,日的 共价数为1, O的共价数为2, H—O键的共用电子对偏移于O, 因此H的氧化值为+ 1, O—O键的共用电子对不发生偏移,此两个O的氧化值总数为-2,平均每个O的氧化值为-1,这与氧的共价数就不一致了。
要确定化合物中某元素原子的氧化值时,只要按照化合物中,所有元素原子的正氧化值和负氧化值的代数和等于零的规则,就可计算出某元素原子的氧化值。例如在硫代硫酸钠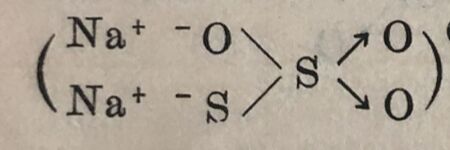 中,已知Na的氧化值为+1,O的氧化值为-2,可以计算出S的氧化值应等于+2;同样,在连四硫酸
中,已知Na的氧化值为+1,O的氧化值为-2,可以计算出S的氧化值应等于+2;同样,在连四硫酸
钠( Na₂S₄O₆)中,可计算出S的氧化值为2/5或2.5。
从上述讨论可以看出,元素的氧化值可以是整数,也可以是分数,而电价或共价数则只有整数。
氧化值的概念,常用于氧化还原反应化学方程式的配平。











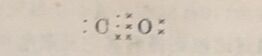
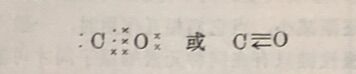
 .
.