举例来说,假定在一只1升容器中我们有压力为100毫米的气体A,和在另一只1升容器中又有压力为100毫米的气体B。将
气体B转移到装有气体A的的1升容器中去之后,温度保持不变,发现混合物的总压力是200毫米。可以合乎逻辑地假定每种气体所施的压力同以前一样。在气体混合物的组成间不发生化学反应时,毎种气体的压力彼此互不发生干扰。在混合物中各气体的压力叫做该气体的分压。气体混合吻的总压力等于混合物中所有气体分压力的总和。这个定律叫做道尔顿分压定律,它可以叙述如下:气体混合物的总压力等于组成气体的分压カ之和。
.jpg) 测量一定体积气体或混合气体压力的方便方法是排水取气法,并使它的压力等于当时的空气压力。这是容易做到的,只要调整水平面2(图10-8)使之容器内外一样,此时气体存在的大气压力可以从实验室大气压计上读出。
测量一定体积气体或混合气体压力的方便方法是排水取气法,并使它的压力等于当时的空气压力。这是容易做到的,只要调整水平面2(图10-8)使之容器内外一样,此时气体存在的大气压力可以从实验室大气压计上读出。
不过用这个方法来确定压力时,还有另一个因素需要加以考虑。当排水收集气体时,它会很快被水蒸气饱1,在20°0时,大气压压760毫米和。混合物的总压力将等于气体分压2.在20°C时,气体和水蒸气压和水蒸气分压的总和。于是纯气体的压力等于总压力减去水蒸气压力。
假定在26°0和750毫米压力下在水面上收集了200毫升的氢气。在26°时的水蒸气压力是25毫米。问在26°时干燥氢气的压力是多少?
根据道尔顿分压定律,干燥氢气的压力是总压力(750毫米)与在26°时水蒸气压力(25毫米)的差值,或即,
Ph2=P总-P水蒸气=750毫米一25毫米=725毫米
.jpg)
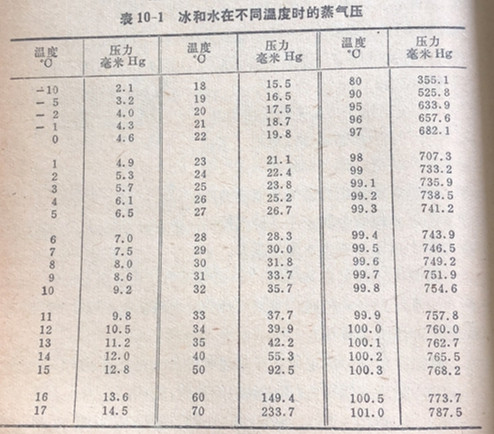
在各温度下水的蒸气压提供在表10-1中。这个表和图10-9说明了一个事实,即蒸气压是随温度的升高而增加的。
相关文章
道尔顿原子学说和新元素的发现https://www.999gou.cn/article.php?id=1661
