




已知的各种元素在它们们的物理和化学性质上以及由它们所形成的化合物的性质上都有极大的差异。对于元素的各种性质以及它们的许多化合物进行学习是极费力的和非常费时间的。尽管每个元素都与每个其它元素不同,但仍可依元素的相似性进行分类从而简化了我们的学习。这种广为采用的分类法叫做周期表。
早在化学发展的初期人们就已经清楚,根据当时已知的某些元素的类似性可以把它们互相划分成组。具有类似性质的元素组的例子有锂、钠和钾(现在叫做碱金属族的一部分),钙、锶和钡(在碱土金属族中)和氯、溴和碘(在卤族中)。
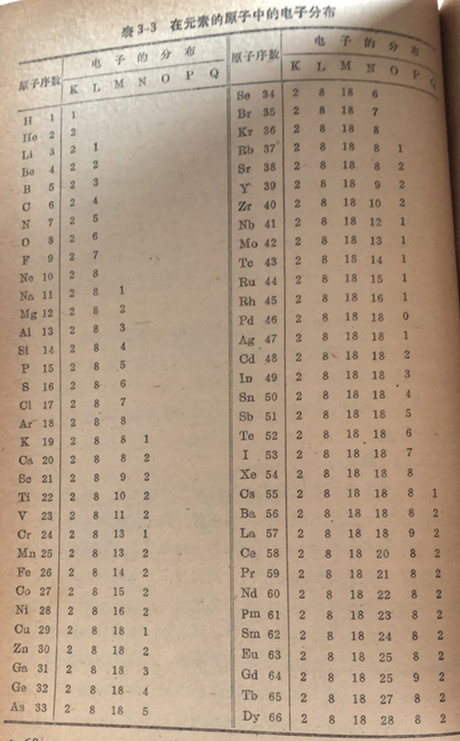
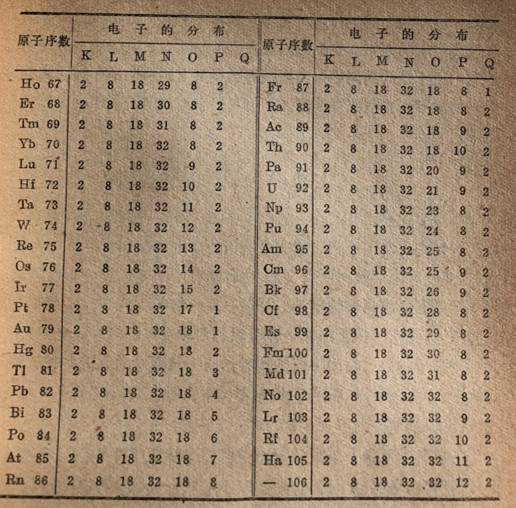
德国化学家杜伯菜纳(D6 berner)在1829年首次提出在元素的原子量和性质之间存在着一种关系。他指出锶的原子量大致处在两个化学性质相似的元素钙和钡的原子量的中间,并且锶的性质也介于钙和钡之间。后来他又认识到还存在着类似元素的其它三素组。在这些三素组中有氯、溴和碘碘;以及、钠和钾等三素组。在1854年其他化学家指出氧、硫、硒和碲可划分成一个元素素族,而氮、璘、砷、锑和铋可组成另一个元素族。
在1865年英国的牛兰斯( Newlands)认识到在元素原子量大小和元素的性质之间有一种相互关系。在1870年俄国的门列
夫( Mendeleev)和德国的麦耶( Lothar Meyer)分别独立地和显然不知道牛兰斯的工作,对元素性质和原子量之间关系的本性作了较为详细的概括。他们的结论导致了如下的叙述:元素的性质是它们原子量的周期函数。这种思想可用下列两个系列的元素为例来加以说明。请注意这些元素从左到右是按原子量递增的顺序而排列的。

这两行元素包含了近代周期表中所谓的第二周期和第三周期的元素(表表3-4和本书前封面背页)。在各横行中的元素彼此在物理和化学性质上都有明确的差异。不过在一个给的横行中,随着原子量的增大,元素的性质出现一种有意思的和有用的渐变。此外,当元素按原子量增加的顺序而排列时,同一纵列中的元素有相类似的性质。举例来说,锂(Li)在物理和化学性质上极相似于钠(Na)和铍(Be)极类似于镁(Mg)。
在氩之后下一个较重的元素是钾,它类似于锂和钠。不过从钾开始到铷(它类似于钾)之间按原子量增加的顺序必须加入18个元素。这18个元素组成一个长周期,以同从锂和钠开始的两个短周期相区别。其它的长周期提供在周期表中。在第3.14节中从原子结构出发对长周期和短周期的外貌作出了解解释。
莫斯莱(第3.7节)的工作指出对于确定元素的化学性质来说基本因素是原子序数而不是原子量。如果你考考察一下周期表的排列,你将会注意到氩(原子量39.948)排在钾(原子量39.098)之前,钻(原子量59.9332)排在镍(原子量58.70)之前,碲(原子量127.60)排在碘(原子量126.9045)之前,钍(原子量232.0381)排在镤(原子量231,0359)之前,以及铀(原子量238.029)排排在镎(原子量237.0482)之前。这些根据原子量的颠倒现象是由于这许多对元
素的反常同位素百分比造成的。举例来说,让我们来考虑(原子序数18)和钾(原子序数19)。这些元素的的同位素丰度使氩的天然存在同位素混合物的原子量重量平均值大于钾的。例如,几乎完全由质量数为40的同位素所组成,但钾大部是由质质量数为39的同位素所组成。如果元素是按原子序数的递增而排列的话,上述的这十个元素就将排在周期表中的恰当位置上。周期律的近代叙述形式是:元素的性质是它们原子序数的周期函数。