





氧的元素符号是O,原子量是16.氧气的分子式是O2,分子量是32.
氧气的物理性质是氧气是无色、无味、无嗅的气体,比空气略为重些,在0°C和1大气压下,1升氧气重1.429克(1升空气重1.293克),在增加压强和降低温度时,氧气也能变成液态的甚至固态的.液态氧是一种淡蓝色的液体,它在-183°c时沸腾,并在-219C时凝成淡蓝色的固体。
①氯气在0℃和1大气压下每升重0.178克,是同体积空气重的17左右
氧气在水中较难溶解.在20℃和1大气压下,1升水只能溶解0.03升的氧气,这些溶解在水里的氧气,对维持水生动物的生命有着重要的作用。
氢气的化学性质
1.氧气和非金属的反应
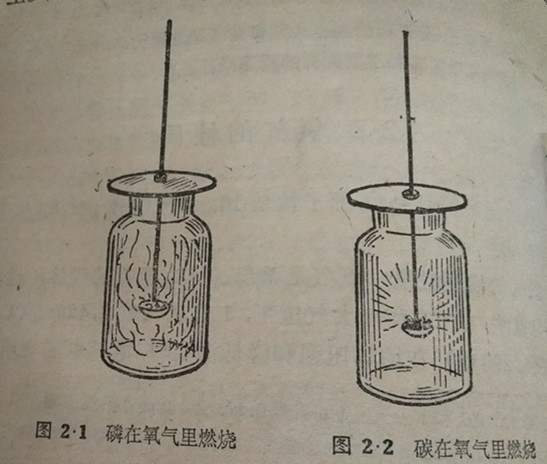
(1)把赤磷(由磷元素组成的一种红褐色粉末状的单质)放在燃烧匙里,在酒精灯上加热,它能在空气里燃烧,并发出微弱的火光,如果把燃着的磷插入充满氧气的集气瓶里(图2·1),这时磷的燃烧就比在空气里剧烈得多,发出的光也明亮得多.同时瓶里充满了白烟,稍过一些时候候,白烟慢慢消失,在瓶壁上附着一层白色的粉末.这种白色固体是磷和氧气发生反应以后生成的新物质,叫做五氧化二磷,它的分子式是:
P2O5。从这个分子式可以看出,五氧化二磷的分子是由2个磷磷原子和5个氧原子结合而成的,这个化学反应,可以用下面的式子来表示:
磷+氧气>>>点燃>>>五氧化二磷
(P)(O2) (P2O5)
在这种式子里,记号“→>”上面,注明了发生这一反应所需的条件,例如必须先把赤磷“点燃”(这就是条件)后,再放入氧气瓶里,赤磷才会和氧剧烈化合,生成五氧化二磷,否则,上述反应是不会发生的.
(2)木炭(它的主要成分是碳)在空气里虽然也能燃烧,但只能发出暗红的光.如果把燃着的木炭放进充满氧气的集气瓶里(图2·92), 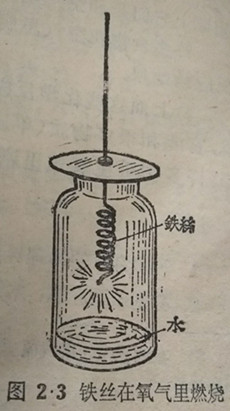 这时木炭燃烧得更加旺盛,发出较强的光辉.在木炭燃烧过的那只集气瓶里,如果倒入一些澄清的石灰水,石灰水立刻变得混浊,这证明瓶子里有二氧化碳存在(见§3·4).二氧化碳是碳和氧气发生反应以后生成的新物质,它的分子式是CO2.这个化学
这时木炭燃烧得更加旺盛,发出较强的光辉.在木炭燃烧过的那只集气瓶里,如果倒入一些澄清的石灰水,石灰水立刻变得混浊,这证明瓶子里有二氧化碳存在(见§3·4).二氧化碳是碳和氧气发生反应以后生成的新物质,它的分子式是CO2.这个化学
反应,可以用下面的式子表示:
碳+氧气>>>点燃>>>二氧化碳
(C)(O2) (CO2)
除了上面所讲的磷和碳外,大多数的非金属都能在一定条件下和氧气发生反应.例如,氢气在氧气里燃烧生成水(H2O),硫在氧气里燃烧生成二氧化硫(SO2),等等.
2.氧气和金属的反应绝大多数的金属(除金、铂等少数几种外,也都能和氧气反应,有些化学性质比较活浚的金属(例如钠、钾等),在平常温度下就能和氧气迅速反应,有些金属在高温时能够在纯粹的氧气里剧烈地燃烧起来.例如铁,一般说来在空气里是不能燃烧的,但在纯氧里却可以燃烧,这可以从把一根细铁丝盘成螺旋状,铁丝一端绰一根火柴梗,把火柴梗点燃下面的实验观察得到。
把一根细铁丝盘或螺旋状,铁丝一端缚一根火柴梗,把火柴梗点燃后,立即将铁丝插入氧气瓶里①,这时被火柴梗烧热的铁丝在纯氧里发生猛烈的燃烧,由于燃烧时产生很多热量,使燃着的铁丝被灼热成白状态,发出强烈的白光,火花四射(图2-3),生成了四氧化三三铁,它的分子式是FeO4.这个变化可以用下面的式子来表示:
氧气 + 铁>>>灼热>>>四氧化三铁
(O2) (Fe) (Fe3O4)
3.氧气和化合物的反应氧气除了能和多种单质(非金属和金属)发生反应外,还能和某些化合物,特别是含碳的化合物发生反应.我们知道,木柴、酒精、煤气(在这些物质里都包含有含碳的化合物)等常用作燃料,都能够在空气里燃烧,实际上它们是和空气里的氧气发生反应.
许多食物在空气里腐败,也是食物和空气里的氧气发生反应的结果.
从上面这些化学反应,可以看出氢气的化学性质非常活,它能和很多物质(单质和化合物)发生反应,在反应的过程里,许多物质在氧气里剧烈地燃烧起来,并出大量的热。
