分子式的意义和写法我们知道,物质的分子是由原子组成的,原子可以用元素符号来表示,因此,利用元素符号也可以表示物质的分子组成。
用元素符号来表明物质分子组成的式子叫做分子式。
根据定组成定律,每一种纯净物质都有固定不变的组成因此,表示每一种物质组成的分子式,也只能有一个.这就是说,纯净物质的分子式,也是固定不变的。
单质的分子是由同种原子组成的,某些单质的分子是由单个原子组成的,例如氨气、氖气等惰性气体(见§21),叫做单原子分子.很显然,这些物物质的分子,实质上就是单个原子,因此,这一类单质的分子式,就是构成这种分子的原子的元素符号.例如:
氨原子的元素符号是He,氯气的分子式也是He;
氖原子的元素符号是Ne,氖气的分子式也是Ne;等等,
另一些单质的分子是由2个相同的原子组成的,例如,氧气的分子是由2个氧原子组成,氮气的分子是由2个氮原子组成,氢气的分子是由2个氢原子组成,等等.这些分子叫做双原子分子.书写这类单质的分子式时,要要在组成这种单质的元素符号的右下角,注上一个较小的“2”字(表示这种单质的每一个分子里含有2个原子).例如:
氧气的分子式的O2(读作O-2);
氮气的分子式是N2(读作N一2);
氢气的分子式是H2(读作H-2);等等
还有一些单质的分子,它们是由很多很多个相同的原子组成的,例如许多金属的和某些固体的非金属(如碳、硅等)的分子,这类单质的分子式,现在习惯上用它们的元素符号来代表.例如:
汞的分子式用汞的元素符号Hg来代表;
铁的分子式用铁的元素符号Fe来代表;
碳的分子式用碳的元素符号C来代表;等等
化合物的分子是由不同种原子组成的.要书写化合物的分子式,首先必须知道化合物的组成,也就是这种化合物含有哪几种元素,以以及这种化合物的每一个分子里的每种元素各有多少个原子.知道了这些以后(这可以通过实验方法来测定),就可以依次把这些元素和表明每种元素的原子的数目(表示的方法也是在元素符号的右下角用一个小的数字注明)写出来,这样就得到了这种化合物的分子式。

例如,每个水分子含有2个氢原子和1个氧原子,水的分子式应写成H20(读作H-2-0);
每个二氧化碳分子含有1个碳原子和2个氧原子,二氧化碳的分子式应写成CO2(读作C-0-2);
①分子里如果含有某元素只有1个原子的,就不必在元素符与号的右下角1”字,例如水的分子式不写成H2O1而写成H2O.
每个硫酸分子含有2个氢原子、1个硫原子和4个氧原子,硫酸的分子式应写成H2SO4(读作Hー2-S-O一4);等等。
由此可以看出,分子式首先代表:
(1)某某种物质
(2)某种物质的一个分子
例如,分子式H2SO,它代表“硫酸”这种物质和硫酸的1个分子.如果分子式前面添上一个系数,就表示不止一个分子,例如2H2O、3C02分别表示2个水分子、3个二氧化碳分子。
其次,分子式还表示该物质的组成,它包含有两方面的意义,即:
(1)表明这种物质是由哪几种元素组成的
(2)表明在这种物质的1个分子里,含有各种原子的个数.例如如,分子式且2SO,它表示硫酸是由氢、硫、氧三种元素组成的,并且还表示在1个硫酸分子里含有2个氢原子、1个硫原子和4个氧原子。
书写化合物的分子式时,要按照一定的顺序,例如水的分子式一定要写成H2O,不能写成OH2,虽然这两个式子所表示的水的组成的意义是相同的,但“OH2”这样的写法是不符合水分子式的规定写法的,因此也是错误的,.关于各类不同化合物分子式的写法,我们将在第五章里详细讨论。
在分子式里,元素符号右下角注的小字不能随便移到元素符号的前面,因为它们代表的意义不同.例如,氧气的分子式O2它表示每1个氧气分子是由2个氧原子组成的,但20并不是氧气的分子式,它代表2个氧原子,这2个氧原子并没有结合成为氧分子。
分子量我们知遺,分子是由原子组成的,分子式既然能表示出物质每个分子里所含各种原子的个数,因此,根据分子有结合成为氧分子
式可以算出分子量,方法是把组成这种分子的所有原子的重量(用原子量来表示)都加起来,例如,二二氧化碳的分子式是CO2,这表明每一个二氧化碳分子是由1个碳原子和2个氧原子所组成,已知碳的原子量是12,氧的原子量是16,因此,二氧化碳的分子量应为1×12+2X16=44.可见,分子式除了表明前面所讲的几种意义以外,还代表物质的分子量,分子量就是组成这种分子的所有原子的原子量的总和,它和原子量一样,也是没有单位的。
从上面所讲的可以看出,如果已经知道了物质的分子式我们就可以很方便地计算出它的分子量.但是物质的分子式是怎样知道的呢?关于这个问题,在本丛书化学第三册第六章里将详细介绍.这里只先说明一下,在确定物质分子式时,般都要先求出分子量.因此,实际情况是:分子量不是由分子式求出,恰恰相反,分子式是由分子量来确定的.而物质的分子量是通过实验来测定的.用实验测定物质分子量的方法,也将在第三册第六章里介绍。
根据化合物分子式的计算分子式既代表物质的组成因此,根据分子式可以计算有关物质组成方面的一些问题。
1.由分子式计算各种元素在化合物里的重量比根据化合物的分子式,可以算出1个分子里各种元素的重量比,例如,二氧化碳的分子式是CO2,它表示在每1个二氧化碳分子里含有1个碳原子和2个氧原子.从碳和氧的的原子量可知1个碳原子重12,1个氧原子重16.因此,在1个二氧化碳的分子里,碳元素和氧元素的重量比是:
(1×12):(2×16)=12:32=3:8
因为纯净物质是由同一种分子组成的,1个分子里各种元素的重量比,必然也就是这化合物里各种元素的重量比.因此,在二氧化碳里,碳、氧两种元素的重量比也是3:8。
由上面的计算可以看出:在化合物里各种元素的重量比,就是化合物分子里各元素的原子个数和它原子量的乘积的比。
2.由分子式计算化合物里各元素的重量百分比元元素在化合物里的重量百分比就是每100重量单位的化合物里所含该元素的重量单位数,常用符号%来表示,例如,已知在每100克水里,含有氢元素11.12克和氧元素88.88克,氢、氧两元素在水里的重量百分比就分别是11.12%和88.88%。
由化合物的分子量以及化合物分子里所含各元素的重量(=原子个数×原子量),可以求出它们的重量百分比。
例如,根据二氧化碳的分子式,可以求出它的分子量
M1=1×12+2×16=44,
其中,所含碳元素的重量是1×12=12;所含氧元素的重量是
2×16=32
在100分重量的二氧化碳里所含碳元素的重量(假设为x和氧元素的重量(假设为y),可以通过下面的比例方法求得:

即碳元素的重量百分比是27.3%,氧元素的重量百分比是72.7%。
①M在化学上常用作分子量的符号
在求出碳元素的重量百分比后,氧元素的重量百分比也可由下法法求得:
100%一碳元素的重量百分比=100%-27.3%=72.7%
由上面的计算可以看出:化合物里基元素的重百分比等于:
化物分子里某元素的原子个数x原子感×100)%
化合物的分子量
例1.求硫酸(分子式H2SO2)里氢、硫、氧三种种元素的重量百分比(氢的原子量=1,硫的原子量=32,氧的原子量=16)。
【解】硫酸的分子量=2×1+1×32+4×16=98,
氢元素的重量百分比=(98×100)%=2.04%,
硫元素的重百分比=(82×x10)%=32,65%
氧元素的重量百分比=(4×1x100)%=65,31%.
答:硫酸里氢、硫、氧三种元素的重量百分比分别是2,04%,32.65%和65.31%。
3.由分子式计算一定重量的化合物里所含某元素重量在求出化合物里某元素的重量百分比后,就可求出,重量的化合物里所含该元素的重量,它等于。
化合物的重量×某元素的重量百分比,
或,化合物的重量x(某元素的原子个数×原子量
化合物的分子量 ×100)%
例2.求22克二氧化碳里碳元素的重。
【解】二氧化碳的分子量=1×12+2×16=44,
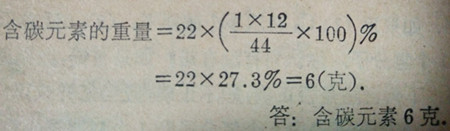
答:含碳元素6克
例3.多少克水里所含的氢元素和10克硫酸里所含的氢元素的重量刚好相等?
【解】根据前一个例题和上面的公式,

答:1,836克水里所含的氢元素和10克硫酸里所含的氢元素相等。

补充资质:化学式和分子式的区别;分子式是用于表示物质的实际组成。例如:氯化氢的化学式为HCl,其实际意义是表示一个氯化氢是由1个Cl跟1个H组成。
化学式是我们为了简便将物质元素组成数约分保留其最简比,化学式是实验式、分子式、结构式、示性式的统称。例如:氯化氢的化学式为HCl(其目的是为了简便,因为有的物质如果写成分子式非常复杂)。
化学式:纯净物都有一定的组成,都可用一个相应的化学式来表示其组成(每种纯净物质的组成是固定不变的,所以表示每种物质组成的化学式只有一个。有些化学式还能表示这种物质的分子构成,这种化学式也叫作分子式。化学式仅表示纯净物,混合物没有化学式。
例如:根据化学式NaCl,就知道,氯化钠是由氯元素和钠元素组成的。
分子式:有些物质确实由分子构成,在分子内原子间以共价键联结,而分子间以范德华力或氢键联结,这些物质就具有分子式。
分子式不仅表示了物质的组成,更重要的,它能表示物质的一个分子及其成分、组成(分子中各元素原子的数目、分子量和各成分元素的重量比)。
化学式:化学式包含分子式,分子式是用元素符号表示纯物质(单质和化合物)的分子组成和相对分子质量的化学式。
分子式:通常分子晶体有分子式,而离子晶体、原子晶体、金属没有分子式。分子式必须是对于那些含有分子的物质来说的。
比如:根据分子式NaCl可知,氯化钠是由一个氯元素和一个钠元素组成的。