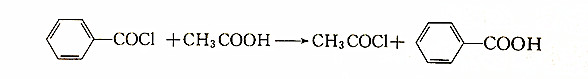与不饱和烃的酯化反应 烯烃与无水乙酸作用可得到乙酸酯,通常是仲醇或叔醇类的乙酸酯。如丙烯可得乙酸异丙酯,异丁烯则得乙酸叔丁酯。少量水能抑制这类反应。烯烃在铂等贵金属催化剂存在时,经氧化和酯化反应能生成不饱和酯,如乙烯、空气、乙酸通过钯-乙酸锂催化剂时即生成乙酸乙烯酯:
CH2=CH2+1/2O2+CH3COOH → CH2=CHOOCCH3+H2O
丁二烯、丙烯和其它不饱和烃都可进行类似的反应。改变工艺条件或催化剂可以制备乙二醇二乙酸酯。例如,乙烯用二氧化鍗和氢溴酸为催化剂进行氧化和酯化时即生成乙二醇二乙酸酯,后者可热分解为乙酸乙烯酯:

三价锰盐或其它锰盐与一种氧化剂存在时。乙酸与高级烯烃作用生成烷基丁内酯,如与1-庚烯反应即生成戊基丁内酯:
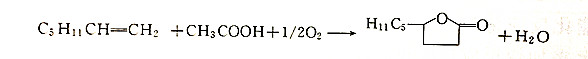
乙炔和乙酸用乙酸汞为催化剂可生成乙酸乙烯酯,此法现在已无工业价值,当有过氧化叔丁基存在时,乙炔与乙酸反应得己二酸:
HC≡CH+2CH3COOH → HOOC(CH2)4COOH
醇醛缩合反应 以硅铝酸钙钠[含钙的造沸石(Decalso)]或负载氢氧化钾的硅胶为催化剂时,乙酸与甲醛缩合得丙烯酸:
CH3COOH+HCHO → CH2=CH—COOH+H2O
甲醛单程转化率50%~60%,而收率可达80%~100%。用此方法生产丙烯酸比其它路线能耗大,在工业上没有进一步应用。
与金属氧化物或碳酸盐反应 醋酸是弱酸,其酸性比碳酸略强。很多金属的氧化物、碳酸盐溶解于醋酸能生成简单的醋酸盐。碱金属的乙酸盐的制备就是以相应的碱金属氧化物或碳酸盐与乙酸直接作用而成,其反应速度虽不及硫酸或盐酸,但较其它大多数有机酸要快得多。过渡金属的乙酸盐可直接以金属与乙酸反应,如添加少量的氧化剂可以促进金属的溶解。
乙酸溶液中通过电流可使铅棒加速溶解生成四乙酸铅,甚至一些贵金属在电流的影响下也能溶解于乙酸。
熔融状的碱金属和碱土金属乙酸盐的混合物骤冷后形成透明的玻璃状固体,它能掺入乙酸而不失其玻璃状结构。这种玻璃能完全溶解于水,在紫外线照射时能发出蓝色或青色荧光。
醋酸的水溶液腐蚀性极强,10%(质量)左右的醋酸水溶液对金属腐蚀性最大,常用的食用醋和工业冰醋酸的腐蚀性都比较低,这为工业生产和家庭烹调带来方便。
分解反应 乙酸燃烧时发出蓝色火焰,燃烧产物是二氧化碳和水。热的浓硫酸能使乙酸脱水炭化,放出二氧化碳和少量的二氧化硫。在Pt/C催化剂作用下,乙酸在227~527℃,在低压条件下分解,得到乙烯酮、甲烷、二氧化碳等产物。干燥的乙酸蒸馏时生成少量的乙酸酐。如果没有催化剂,沸腾7h达到平衡,如果有微量的酸性催化剂,20min就能达到平衡。平衡时每升乙酸含有4.2mmol乙酸酐。乙酸经乙烯酮合成乙酸酐是乙酸酐的工业生产方法。
CH3COOH → CH2=C=O+H2O
CH2=C=O+CH3COOH → (CH3CO)2O
乙酸光化分解生成甲烷、二氧化碳和一些游离基,其反应机理比较复杂。电子撞击和γ射线照射也得到相同的产物。
纯乙酸的电导率极低,在其中加入少量的水,电导率就会发生显著的变化。当加入少量的硫酸时电流则可顺利地通过,并发生分解反应,分解产物为二氧化碳、一氧化碳和氢。电解醋酸盐的水溶液时,在阳极会产生乙烷、二氧化碳和乙烯。
酸-碱性 乙酸是典型的一价弱酸,25℃下在水中的解离常数是pKa=4.76。可用于水中极弱的碱的定量分析。能直接与一些金属氧化物和氢氧化物发生反应生成乙酸盐;又如铅一类的金属还能生成碱式乙酸盐。某些金属的乙酸盐能溶于乙酸,与一个或多个乙酸分子结合形成乙酸的酸式盐,如CH3COONa·CH3COOH.
当用石灰石或菱镁矿中和乙酸的粗品焦木酸时,得到氧化钙的乙酸盐或氧化镁的乙酸盐。乙酸只能接受硝酸、硫酸这些强酸的质子。其它一些非常强的酸,如超强酸,在乙酸中仍表现出强酸性,可以作为乙酸与烯烃或醇进行酯化反应的催化剂。
由于乙酸具有一定的酸性,在乙酸溶剂中进行硝化时,能生成硝离子NO2+,使硝化能够进行。这种硝基阳离子对苯酚的硝化反应比单用硝酸的硝化反应快得多。六亚甲基四胺在乙酸溶剂中可以被硝化生成有爆炸性的环三亚甲基三硝基胺,也称为“旋风炸药”或RDX。
氯代反应 醋酸能在光催化下与氯气发生光氯化反应,生成α-氯代醋酸,氯原子取代醋酸的α-氢类似于自由基连锁反应,可发生多个氯原子的取代衍生物。
CH3COOH+Cl2 → CH2ClCOOH+HCl
CH3COOH+2Cl2 → CHCl2COOH+2HCl
CH3COOH+3Cl2 → CCl3COOH+3HCl
酰化和胺化反应 醋酸和三氯化磷反应生成乙酰氯,和氨反应生成乙酰胺。
3CH3COOH+PCl3 → 3CH3COCl+P(OH)3
CH3COOH+NH3 → CH3CONH2+H2O
乙酸与苯甲酰氯反应得乙酰氯: